Giải bài tập SBT Hóa 11 Bài 30: Ankađien
Dựa theo nội dung SBT Hóa học 11 eLib xin giới thiệu đến các em học sinh bài giải Ankađien. Bài này sẽ giúp các em nắm vững được lý thuyết cũng như cách giải các bài tập đầy đủ, chi tiết và rõ ràng. Hy vọng đây sẽ là tài liệu tham khảo hữu ích với các em học sinh.
Mục lục nội dung

1. Giải bài 6.14 trang 44 SBT Hóa học 11
Cho isopren (2-metylbuta-1,3-đien) phản ứng cộng với brom theo tỉ lệ 1:1 về số mol. Số đồng phân cấu tạo có cùng công thức phân tử C5H8Br2 tối đa có thể thu được là
A. 1
B. 2
C. 3
D. 4
Phương pháp giải
Xem lại lí thuyết về Ankađien
Do mang liên kết đôi C=C trong phân tử nên ankađien cũng có phản ứng đặc trưng là phản ứng cộng.
Các phản ứng cộng xảy ra với ankađien cũng tương tự như ở anken.
Tuy nhiên vì có chứa 2 liên kêt đôi C=C nên ankađien có thể tham gia phản ứng cộng theo tỉ lệ mol 1:1 hoặc 1:2.
Hướng dẫn giải
Isopren: CH2=C(CH3)-CH=CH2.
Khi cho tác dụng với Br2 theo tỉ lệ 1:1 có thể có các sản phẩm:
CH2Br-C(Br)(CH3)-CH=CH2; CH2=CH(CH3)-CH(Br)-CH2Br; CH2Br -C(CH3)=CH-CH2Br
Đáp án cần chọn là C.
2. Giải bài 6.15 trang 44 SBT Hóa học 11
Trong các chất dưới đây, chất nào được gọi tên là đivinyl ?
A. CH2 = C = CH - CH3
B. CH2 = CH - CH = CH2
C. CH2 = CH - CH2 - CH = CH2
D. CH2 = CH - CH = CH - CH3
Phương pháp giải
Nắm vững tên gọi và công thức của ankađien.
Hướng dẫn giải
CH2 = CH - CH = CH2 có tên gọi là đivinyl.
→ Đáp án B
3. Giải bài 6.16 trang 44 SBT Hóa học 11
Các nhận xét sau đây đúng hay sai ?
1. Các chất có công thức CnH2n-2 đều là ankađien.
2. Các ankađien đều có công thức CnH2n-2
3. Các ankađien đều có 2 liên kết đôi.
4. Các chất có 2 liên kết đôi đều là ankađien.
Phương pháp giải
Xem lại lí thuyết về Ankađien
- Ankađien là những hiđrocacbon không no, mạch hở trong phân tử có chứa 2 liên kết đôi còn lại là các liên kết đơn.
- Công thức tổng quát: CnH2n-2 (n ≥ 3).
- Danh pháp thay thế: số chỉ vị trí nhánh + tên nhánh + tên mạch chính + a + số chỉ vị trí nối đôi + đien.
Hướng dẫn giải
1 - Sai
2 - Đúng
3 - Đúng
4 - Sai
4. Giải bài 6.17 trang 44 SBT Hóa học 11
Viết công thức cấu tạo của:
1. 2,3-đimetylbuta-1,3-đien
2. 3-metylpenta-1,4-đien
Phương pháp giải
Học sinh nắm vững cách gọi tên và cách viết công thức cấu tạo của hợp chất hữu cơ.
Hướng dẫn giải
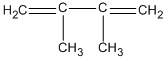 (2,3-đimetylbuta-1,3-đien)
(2,3-đimetylbuta-1,3-đien)
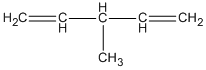 (3-metylpenta-1,4-đien)
(3-metylpenta-1,4-đien)
5. Giải bài 6.18 trang 44 SBT Hóa học 11
Chất A là một ankađien liên hợp có mạch cacbon phân nhánh. Để đốt cháy hoàn toàn 3,4 g A cần dùng vừa hết 7,84 lít O2 lấy ở đktc. Hãy xác định công thức phân tử, công thức cấu tạo và tên của chất A.
Phương pháp giải
Tính theo PTHH: \({C_n}{H_{2n - 2}} + \dfrac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n - 1){H_2}O\)
→ Giá trị của n → CTPT cần tìm.
Viết CTCT và gọi tên A.
Hướng dẫn giải
\({C_n}{H_{2n - 2}} + \dfrac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n - 1){H_2}O\)
Theo phương trình : Cứ (14n - 2) g ankađien tác dụng với \(\dfrac{{3n + 1}}{2}\) mol O2.
Theo đầu bài : Cứ 3,4 g ankađien tác dụng với 0,35 mol O2.
\(\dfrac{{14n - 2}}{{3,4}} = \dfrac{{3n - 1}}{{2.0,35}} \Rightarrow n = 5\)
Công thức phân tử: C5H8
Công thức cấu tạo: CH2=C(CH3)-CH=CH2 (2-metylbutan-1,3-ddien hay isopren)
6. Giải bài 6.19 trang 44 SBT Hóa học 11
Hỗn hợp khí A chứa một ankan và một ankađien. Để đốt cháy hoàn toàn 6,72 lít A phải dùng vừa hết 28 lít O2 (các thể tích lấy ở đktc). Dẫn sản phẩm cháy qua bình thứ nhất đựng H2SO4 đặc, sau đó qua bình thứ hai đựng dung dịch NaOH (lấy dư) thì khối lượng bình thứ nhất tăng p gam và bình thứ hai tăng 3,52g.
1. Xác định công thức phân tử và phần trăm theo thể tích của từng chất trong hỗn hợp A.
2. Tính giá trị p.
Phương pháp giải
Giả sử trong 6,72 lít A có x mol CnH2n+2 y mol CmH2m-2.
Viết các PTHH:
\({C_n}{H_{2n + 2}} + \dfrac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
\({C_m}{H_{2m - 2}} + \dfrac{{3m - 1}}{2}{O_2} \to mC{O_2} + (m - 1){H_2}O\)
Khai thác dữ kiện đề bài, lập hệ pt tìm x, y, n, m => Trả lời yêu cầu của bài toán.
Hướng dẫn giải
Giả sử trong 6,72 lít A có x mol CnH2n+2 y mol CmH2m-2.
\(x + y = \dfrac{{6,72}}{{22,4}} = 0,3(1)\)
\({C_n}{H_{2n + 2}} + \dfrac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
x mol \(\dfrac{{3n + 1}}{2}\)x mol nx mol (n + 1)x mol
\({C_m}{H_{2m - 2}} + \dfrac{{3m - 1}}{2}{O_2} \to mC{O_2} + (m - 1){H_2}O\)
y mol \(\dfrac{{3m - 1}}{2}\)y mol my mol (m - 1)ymol
Số mol O2 : \(\dfrac{{(3n + 1)x + (3m - 1)y}}{2} = \dfrac{{28}}{{22,4}}\) = 1,25 mol)
→ (3n + 1)x + (3m - 1)y = 2,5 (2)
Số mol CO2 : nx + my = \(\dfrac{{35,2}}{{44}}\) = 0,8 (mol)
→ (3n + 1)x + (3m - 1)y = 2,5 (3)
Từ (2) và (3) tìm được x - y = 0,1 ;
Kết hợp với x + y = 0,3, ta có : x = 0,2 và y = 0,1 Thay các giá trị tìm được vào (3) ta có
0,2n + 0,1m = 0,8 → 2n + m = 8.
Nếu n = 1 thì m = 6 : Loại, vì C6H10 không phải là chất khí ở đktc. Nếu n = 2 thì m = 4. Công thức hai chất là C2H6 và C4H6
Nếu n = 3 thì m = 2 : Loại vì m > 3.
Trả lời : Hỗn hợp A chứa C2H6 (66,67%) và C4H6 (33,33%)
Số mol H2O = (n + 1)x + (m - 1)y = 0,9 (mol).
2. Khối lượng nước : p = 0,9.18 = 16,2 (g).
Tham khảo thêm
- doc Giải bài tập SBT Hóa 11 Bài 29: Anken
- doc Giải bài tập SBT Hóa 11 Bài 31: Luyện tập: Anken và ankađien
- doc Giải bài tập SBT Hóa 11 Bài 32: Ankin
- doc Giải bài tập SBT Hóa 11 Bài 33: Luyện tập Ankin