Giải bài tập SGK Hóa 11 Bài 29: Anken
Anken có cấu tạo khác với ankan như thế nào? Điều đó ảnh hưởng đến tính chất hóa học nào của chúng? Để biết chi tiết về điều đó, eLib xin chia sẻ với các bạn nội dung giải bài tập dưới đây với nội dung lời giải chi tiết, hi vọng rằng đây sẽ là tài liệu giúp các bạn học tập tốt hơn.
Mục lục nội dung

1. Giải bài 1 trang 132 SGK Hóa học 11
So sánh anken với ankan về đặc điểm cấu tạo và tính chất hóa học. Cho thí dụ minh họa?
Phương pháp giải
Để giải bài tập này cần nắm vững kiến thức về anken, đồng thời nhớ lại kiến thức về ankan để tiến hành so sánh 2 chất này về đặc điểm cấu tạo và tính chất hóa học.
Hướng dẫn giải
Khác với ankan là phân tử chỉ chứa liên kết xích ma, phân tử anken có chứa 1 liên kết pi kém bền, dễ gẫy, do đó không giống với ankan là cho phản ứng thế là phản ứng đặc trưng, anken cho phản ứng cộng là phản ứng đặc trưng.
Ví dụ:
C2H4 + H2 → C2H6
C2H4 + Br2 → C2H4Br2
C2H4 + HBr → C2H5Br
Ngoài ra anken còn cho phản ứng trùng hợp phản ứng làm mất màu dung dịch thuốc tím.
2. Giải bài 2 trang 132 SGK Hóa học 11
Ứng với công thức C5H10 có bao nhiêu đồng phân cấu tạo?
A. 4
B. 5
C. 3
D. 7
Phương pháp giải
Anken có các loại đồng phân:
- Đồng phân về mạch C:
+ Mạch không phân nhánh
+ Mạch nhánh
- Đồng phân về vị trí liên kết đôi
- Đồng phân cis - trans
Hướng dẫn giải
Chú ý là ứng với công thức CnH2n có anken và xicloankan.
Nếu đề hỏi chung chung thì phải cộng cả hai đồng phân anken và xicloankan lại
Đồng phân anken:
CH2=CH-CH2-CH2-CH3
CH3-CH=CH-CH2-CH3
CH2=CH-CH(CH3)-CH3
CH3-CH=C(CH3)-CH3
CH3-CH2-C(CH3)=CH2
Đồng phân xicloankan:
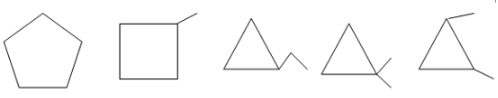
3. Giải bài 3 trang 132 SGK Hóa học 11
Viết phương trình hóa học của phản ứng xảy ra khi:
a) Propilen tác dụng với hidro, đun nóng (xúc tác Ni).
b) But-2-en tác dụng với hirdo clorua.
c) Metylpropen tác dụng với nước có xúc tác axit.
d) Trùng hợp but-1-en.
Phương pháp giải
Để giải bài tập này cần nắm vững kiến thức về anken → Viết phương trình minh họa
Hướng dẫn giải
a) CH2=CH-CH3 + H2 → CH3-CH2-CH3
b) CH3-CH=CH-CH3 + HCl → CH3-CH2-CHCl-CH3
c) CH2=C(CH3)-CH3 + H2O → CH3-C(CH3)2-CH3
d) nCH2=CH-CH2-CH3 → (-CH2-CH(CH2-CH3))n
4. Giải bài 4 trang 132 SGK Hóa học 11
Trình bày phương pháp hóa học để:
a ) Phân biệt metan và etilen.
b ) Tách lấy khí metan từ hỗn hợp etilen.
c) Phân biệt hai bình không dán nhãn đựng hexan và hex-1-en.
Viết phương trình hóa học của các phản ứng đã dùng.
Phương pháp giải
a) Metan thuộc ankan, etilen thuộc anken => dựa vào tính chất hóa học khác nhau của 2 chất này để chọn chất phân biệt được chúng
VD: Dung dịch nước brom
b) Tương tự a)
c) Hexan và hex-1-en cũng 1 chất thuộc ankan và 1 chất thuộc anken => dựa vào tính chất hóa học đặc trưng của chúng để nhận biết
Hướng dẫn giải
a) Lần lượt cho metan và etilen đi qua dung dịch nước brom, chất nào làm dung dịch nước brom nhạt màu thì đó là etilen, chất nào không làm dung dịch nước brom nhạt màu thì đó là metan.
CH2=CH2 + Br2 ( dd màu nâu đỏ) → CH2Br-CH2Br (dd không màu)
CH4 không tác dụng với dung dịch nước brom
b) Cho hỗn hợp khí (CH4 và C2H4) đi qua dung dịch nước brom dư, C2H4 sẽ tác dụng với dung dịch nước brom, khí còn lại ra khỏi bình dung dịch nước brom là CH4.(PTHH như câu a)
c) Lần lượt cho hexan và hex-1-en đi qua dung dịch nước brom
+ Chất nào làm dung dịch nước brom nhạt màu thì đó là etilen
CH2=CH-[CH2]3-CH3 + Br2 ( dd màu nâu đỏ) → CH2Br-CHBr-[CH2]3-CH3 (dd không màu)
+ Chất nào không làm dung dịch nước brom nhạt màu thì đó là hexan vì hexan không tác dụng với dung dịch nước brom
5. Giải bài 5 trang 132 SGK Hóa học 11
Chất nào sau đây làm mất màu dung dịch brom?
A. Butan
B. But-1-en
C. Cacbon đioxit
D. Metylpropan
Phương pháp giải
Để giải bài tập này cần nắm vững tính chất hóa học của ankan và anken
Hướng dẫn giải
Chất làm mất màu dung dịch brom là but-1-en (anken)
Phương trình phản ứng:
H2C=CH-CH2-CH3 + Br2 → CH2Br-CHBr-CH2-CH3
⇒ Đáp án B.
6. Giải bài 6 trang 132 SGK Hóa học 11
Dẫn từ từ 3,36 lít hỗn hợp gồm etilen và propilen (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 4,90gam.
a) Viết các phương trình hóa học và giải thích các hiện tượng ở thí nghiệm trên.
b) Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu.
Phương pháp giải
a) CH2 = CH2 + Br2 → CH2Br – CH2Br
CH2 = CH – CH3 + Br2 → CH2Br – CHBr – CH3
b)
Gọi x,y lần lượt là số mol của C2H4 và C3H6:
\(\left\{ \begin{array}{l}
{n_{hh}} = x + y = 0,15\\
{m_{hh}} = 28x + 42y = 4,9
\end{array} \right. \to \left\{ \begin{array}{l}
x = ?\\
y = ?
\end{array} \right.\)
→ %V C2H4 = ?%
→ %V C3H6 = ? %
Hướng dẫn giải
Câu a:
Các phương trình hóa học của phản ứng:
CH2 = CH2 + Br2 → CH2Br – CH2Br
CH2 = CH – CH3 + Br2 → CH2Br – CHBr – CH3
Giải thích: Dung dịch brom bị nhạt màu do brom phản ứng với hỗn hợp tạo thành các hợp chất không màu. Khối lượng bình tăng do các sản phẩm tạo thành là những chất lỏng.
Câu b:
Gọi x,y lần lượt là số mol của C2H4 và C3H6:
Ta có 3,36 lít hỗn hợp gồm etilen và propilen: nên x + y = (3,36/22,4) = 0,15 (1)
Khối lượng dung dịch sau phản ứng tăng 4,90gam chính là khối lượng của etilen và propen cho vào nên: 28x + 42y = 4,9 (2)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{ \begin{array}{l}
{n_{hh}} = x + y = 0,15\\
{m_{hh}} = 28x + 42y = 4,9
\end{array} \right.\)
=> x = 0,1 mol; y = 0,05 mol
⇒ %V C2H4 = 66,7%
⇒ %V C3H6 = 33,3%
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Bài 30: Ankađien
- doc Giải bài tập SGK Hóa 11 Bài 31: Luyện tập Anken và ankađien
- doc Giải bài tập SGK Hóa 11 Bài 32: Ankin
- doc Giải bài tập SGK Hóa 11 Bài 33: Luyện tập Ankin