Giải bài tập SGK Hóa 11 Nâng cao Bài 16: Phân bón hóa học
Dưới đây là Hướng dẫn giải Hóa 11 SGK nâng cao Chương 2 Bài 16 Phân bón hóa học được eLib biên soạn và tổng hợp, nội dung bám sát theo chương trình SGK Hóa học 11 nâng cao giúp các em học sinh nắm vững phương pháp giải bài tập và ôn tập kiến thức hiệu quả hơn.
Mục lục nội dung

1. Giải bài 1 trang 70 SGK Hóa 11 nâng cao
Cho các mẫu phân đạm sau đây: amonisunfat, amoniclorua, natri nitrat. Hãy dùng các thuốc thử thích hợp để nhận biết chúng. Viết phương trình hóa học của các phản ứng đã dùng.
Phương pháp giải
- Hòa tan ba mẫu vào nước thu dung dịch.
- Cho dung dịch Ba(OH)2 tác dụng với ba mẫu và đun nhẹ
- Cho vụn đồng và H2SO4 loãng tác dụng với dụng với mẫu còn lại
Hướng dẫn giải
Sự khác nhau giữa nhận biết và phân biệt: để phân biệt các chất A, B, C. chất còn lại đương nhiên là D. Trái lại để nhận biết A, B, C, D cần xác định tất cả các chất, không bỏ qua chất nào.
Hòa tan ba mẫu vào nước thu dung dịch.
Cho dung dịch Ba(OH)2 tác dụng với ba mẫu và đun nhẹ.
Mẫu sủi bọt khi màu khai, đồng thời tạo kết tủa trắng là dung dịch (NH4)2SO4
(NH4)2SO4 + Ba(OH)2 → BaSO4↓ + NH3↑ + H2O
Mẫu sủi bọt khí mùi khai, đồng thời tạo kết tủa rắng là dung dịch NH4Cl
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3 + 2H2O
Mẫu còn lại NaNO3
Cho vụn đồng và H2SO4 loãng tác dụng với dụng với mẫu còn lại, thấy xuất hiện khí không màu hóa nâu ngoài không khí ⇒ NaNO3
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO↑ + 4H2O
2. Giải bài 2 trang 70 SGK Hóa 11 nâng cao
Một trong những Phương pháp điều chế canxi nitrat là cho đá vôi hoặc đá phấn tác dụng với axit nitric loãng. Còn amoni nitrat có thể điều chế bằng cách cho amonitrat tác dụng với amonicacbonat. Viết phương trình hóa học và cho biết tại sao các phản ứng này xảy ra hoàn toàn.
Phương pháp giải
Điều chế canxi nitrat: CaCO3 + 2HNO3 → Ca(NO3)2 + CO2↑ + H2O
Điều chế canxi cacbonat: Ca(NO3)2 + (NH3)2CO3 → CaCO3 + 2NH4NO3
Hướng dẫn giải
Điều chế canxi nitrat: CaCO3 + 2HNO3 → Ca(NO3)2 + CO2↑ + H2O
Điều chế canxi cacbonat: Ca(NO3)2 + (NH3)2CO3 → CaCO3 + 2NH4NO3
Các phản ứng trên xảy ra hoàn toàn vì thỏa mãn điều trao đổi ion.
3. Giải bài 3 trang 70 SGK Hóa 11 nâng cao
Từ không khí, than, nước và các chất xúc tác cần thiết, hãy lập sơ đồ điều chế phân đạm NH4NO3.
Phương pháp giải
Sơ đồ điều chế phân đạm NH4NO3
Hướng dẫn giải
Chưng cất không khí thu N2
C + H2O ⇔ CO + H2 (đk: 1050oC)
NH4NO3 được điều chế từ sơ đồ sau đây:
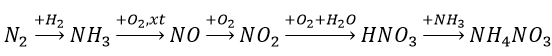
4. Giải bài 4 trang 70 SGK Hóa 11 nâng cao
Tại sao không được trộn supephotphat với vôi? Giải thích rõ và viết phương trình hóa học của phản ứng.
Phương pháp giải
Khi bón phân lân cho cây trồng thì không được trộn supephotphat với vôi bột vì nó làm giảm hàm lượng P2O5 trong phân bón.
Hướng dẫn giải
Vì xảy ra phản ứng sau đây: Ca(H2PO4)2 + Ca(OH)2 → 2CaHPO4 + 2H2O
5. Giải bài 5 trang 70 SGK Hóa 11 nâng cao
Supephotphat được điều chế từ một loại quặng có chứa 73% Ca3(PO4)2, 26% CaCO3 và 1% SiO2.
a) Tính khối lượng dung dịch H2SO4 65% đủ để tác dụng với 100 kg bột quặng đó.
b) Supephotphat đơn thu được gồm những chất nào? Tỉ lệ % P2O5 trong loại pupephotphat đơn trên.
Phương pháp giải
a) Ca3(PO4)2 + 2H2SO4 → 2CaSO4 + Ca(H2PO4)2
CaCO3 + H2SO4 → CaSO4 + CO2 + H2O
Từ phương trình hóa học ta tính được:
- Khối lượng H2SO4 nguyên chất đã dùng
- Khối lượng dung dịch H2SO4 65% đã dùng
b) mCa(H2PO4)2 = ?, nCaSO4 = ?
→ Khối lượng P có chứa trong 55,1 kg Ca(H2PO4)2 ?
→ Khối lượng P2O5 có trong pupephotphat đơn thu được?
→ Tỉ lệ %P2O5 trong loại supephotphat đơn?
Hướng dẫn giải
Câu a: 100kg quặng chứa 73 kg Ca3(PO4)2; 26kg CaCO3; 1kg SiO2
Ca3(PO4)2 + 2H2SO4 → 2CaSO4 + Ca(H2PO4)2
310g 2.98g 2.36g 234g
73kg x kg 64,05kg 55,10kg
CaCO3 + H2SO4 → CaSO4 + CO2 + H2O
100g 98g 136g
26kg y(kg) 35,36 kg
Khối lượng H2SO4 nguyên chất đã dùng là:
mct = x + y = 71,64 kg
Khối lượng dung dịch H2SO4 65% đã dùng:
mdd = (71,64.100) : 65 = 10,22 kg
Câu b: Supephotphat đơn thu được gồm
mCa(H2PO4)2 = 55,1 kg
\({m_{CaS{O_4}}} = \frac{{73.2.136}}{{310}} + \frac{{26.136}}{{100}} = 99,41kg\)
mSiO2 = 1 kg
Khối lượng P có chứa trong 55,1 kg Ca(H2PO4)2 là:
mP = (62.55,1) : 234 = 14,6 kg
Khối lượng P2O5 có trong pupephotphat đơn thu được:
mP2O5 = (14,6.142) : 62 = 33,44 kg
Tỉ lệ %P2O5 trong loại supephotphat đơn trên là:
\(\frac{{3,44.100}}{{99,41 + 55,1 + 1}} = 21,5\% \)
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 9: Khái quát về nhóm Nitơ
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 10: Nitơ
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 11: Amoniac và muối amoni
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 12: Axit nitric và muối nitrat
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 13: Luyện tập Tính chất của nitơ và hợp chất của nitơ
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 14: Photpho
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 15: Axit photphoric và muối photphat
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 17: Luyện tập Tính chất và các hợp chất của photpho