Giải bài tập SGK Hóa 11 Nâng cao Bài 46: Benzen và ankylbenzen
Mời các em cùng tham khảo nội dung giải bài tập Benzen và ankylbenzen được eLib sưu tầm và biên soạn bên dưới đây. Đây là tài liệu tham khảo hay dành cho quý thầy cô cùng các bạn học sinh lớp 9 nhằm phục vụ quá trình giảng dạy và học tập môn Hóa học lớp 11 nâng cao.
Mục lục nội dung
1. Giải bài 1 trang 191 SGK Hóa học 11 nâng cao
2. Giải bài 2 trang 191 SGK Hóa học 11 nâng cao
3. Giải bài 3 trang 191 SGK Hóa học 11 nâng cao
4. Giải bài 4 trang 192 SGK Hóa học 11 nâng cao
5. Giải bài 5 trang 192 SGK Hóa học 11 nâng cao
6. Giải bài 6 trang 192 SGK Hóa học 11 nâng cao
7. Giải bài 7 trang 192 SGK Hóa học 11 nâng cao
8. Giải bài 8 trang 192 SGK Hóa học 11 nâng cao

1. Giải bài 1 trang 191 SGK Hóa 11 nâng cao
Hãy điền chữ Đ (đúng) hoặc S (sai) vào các dấu [...] ở mỗi câu sau:
a) Benzene là một hidrocacbon không no. [...]
b) Benzene là một hidrocacbon thơm. [...]
c) Ở benzene, 3 liên kết đôi ngắn hơn 3 liên kết đơn. [...]
d) Ở bên, 6 liên kết cacbon – cacbon đều như nhau. [...]
e) Ở benzene, 6 C tạo thành một lục giác đều. [...]
g) Ở xiclohexan, 6C tạo thành một lục giác đều. [...]
Phương pháp giải
Nắm vững khái niệm, công thức cấu tạo và đặc điểm của benzen để phân tích từ nhận định từ đó rút ra kết luận
Hướng dẫn giải
a) Sai
b) Đúng
c) Sai
d) Đúng
e) Đúng
g) Sai
2. Giải bài 2 trang 191 SGK Hóa 11 nâng cao
Hãy cho biết vì sao người ta biểu diễn công thức cấu tạo của bezen bằng một hình lục giác đều với một vòng tròn ở trong.
Phương pháp giải
Phân tử benzen gồm 6 nguyên tử H và 6 nguyên tử C nằm trong cùng một mặt phẳng trong đó 6 nguyên tử C tạo thành hình lục giác đều, mỗi nguyên tử C lại liên kết với một nguyên tử H nữa. Độ dài các liên kết C-C bằng nhau, độ dài các liên kết C-H cũng như nhau.
Hướng dẫn giải
Người ta biểu diễn công thức cấu tạo của benzene bằng một hình lục giác đều với một vòng tròn ở trong vì:
- Sáu nguyên tử C trong phân tử benzene ở trạng thái lai hóa sp2.
- Cả sáu nguyên tử C và sáu nguyên tử H của phân tử benzene cùng nằm trên một mặt phẳng.
- Các liên kết C-C có độ dài bằng nhau.
- Các góc hóa trị bằng 120o.
3. Giải bài 3 trang 191 SGK Hóa 11 nâng cao
Những hợp chất nào dưới đây có thể và không thể chứa vòng benzene, vì sao?
a) C8H6Cl2
b) C10H16
c) C9H14 BrCl
d) C10 H12(NO2)2
Phương pháp giải
Để hình thành một vòng benzene phải cần 4 liên kết π: Một liên kết π dùng để làm vòng (một vòng tương ứng với một liên kết π) và 3 liên kết π còn lại nằm trong vòng. Như vậy một hợp chất chứa vòng benzene sẽ có số liên kết π tối thiểu là 4.
Hướng dẫn giải
Hợp chất chứa vòng benzene là C8H6Cl2 và C10H12(NO2)2.
Độ bất bão hòa:
C8H6Cl2 có k = \((\pi + v) = \frac{1}{2}(2.8 + 2 - 8) = 5\)
C10H12(NO2)2 có k = \((\pi + v) = \frac{1}{2}(2.10 + 2 - 14) = 4\)
Hợp chất không chứa vòng benzene là C10H16 và C9H14BrCl
Độ bất bão hòa:
C10H16 có k = \((\pi + v) = \frac{1}{2}(2.10 + 2 - 16) = 3 < 4\)
C9H14BrCl có \(k = (\pi + v) = \frac{1}{2}(2.9 + 2 - 16) = 2 < 4\)
4. Giải bài 4 trang 192 SGK Hóa 11 nâng cao
a) Hãy viết công thức phân tử các đồng đẳng của benzene chứa 8 và 9 nguyên tử C.
b) Viết công thức cấu tạo và gọi tên các đồng phân ứng với các công thức tìm được ở câu a).
Phương pháp giải
Công thức chung của dãy đồng đẳng benzene là CnH2n-6 (n ≥ 6)
Vì các liên kết C-C trong nhân benzen đồng nhất nên benzen chỉ có 3 đồng phân vị trí:
+ Nếu 2 nhóm thế ở 2 C lân cận ta có đồng phân ortho (viết tắt o-) hoặc đánh số 1,2.
+ Nếu 2 nhóm thế cách nhau 1 nguyên tử cacbon (1 đỉnh tam giác) gọi là đồng phân meta (viết tắt m-) hoặc 1,3.
+ Nếu 2 nhóm thế ở 2 nguyên tử cacbon đối đỉnh gọi là đồng phân para (viết tắt p-) hoặc 1,4.
Hướng dẫn giải
Câu a: Công thức chung của dãy đồng đẳng benzene là CnH2n-6 (n ≥ 6)
Công thức phân tử các đồng đẳng của benzene cần tìm là C8H10 và C9H12
Câu b: Công thức cấu tạo của C8H10:
C6H5CH2CH3, C6H4(CH3)2 (o-xilen, m-xilen, p-xilen)
Công thức cấu tạo của C9H12:
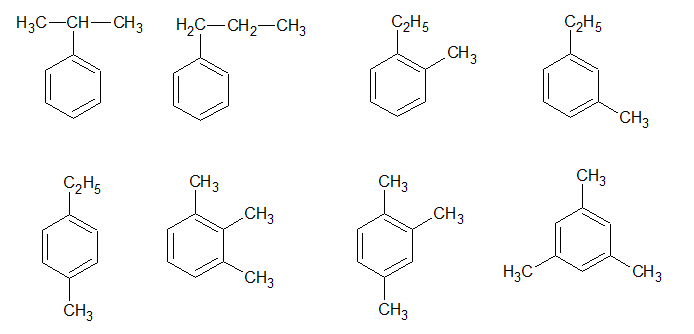
5. Giải bài 5 trang 192 SGK Hóa 11 nâng cao
Viết công thức cấu tạo của các hợp chất sau:
a) etyl benzene
b) 4-cloetyl benzene
c) 1,3,5-trimetyl benzene
d) o- clotoluen
e) m-clotoluen
g) p-clotoluen.
Phương pháp giải
Cần nắm được kĩ năng viết công thức cấu tạo của chất dựa theo tên gọi (trong công thức phải luôn chứa vòng benzen)
Hướng dẫn giải
a) C6H5CH2-CH3
b) C6H4ClC2H5
c) C6H3(CH3)3
d) C6H4ClCH3
e) C6H4ClCH3
g) C6H4ClCH3
6. Giải bài 6 trang 192 SGK Hóa 11 nâng cao
Hãy nêu và giải thích hiện tượng xảy ra trong các thí nghiệm sau:
a) Cho benzene vào ống nghiệm chứa nước brom, lắc kĩ rồi để yên
b) Cho brom lỏng vào ống nghiệm chứa benzene, lắc rồi để yên.
c) Cho thêm bột sắt vào ống nghiệm ở thí nghiệm câu b) rồi đun nhẹ.
Phương pháp giải
- Benzen không tác dụng với nước brom.
- Benzen tham gia phản ứng thế với brom, xúc tác Fe, nhiệt độ
- Lưu ý: brom lỏng là brom nguyên chất là dung môi không phân cực tan tốt trong benzen nên tạo dung dịch đồng nhất.
Hướng dẫn giải
Câu a: Benzene không tác dụng với nước brom.
Vì vậy khi cho benzene vào ống nghiệm chứa nước brom, lắc kĩ rồi để yên. Chất lỏng trong ống nghiệm sẽ tách thành hai lớp: Lớp chất lỏng trên là dung dịch brom trong benzene có màu vàng (phần này do enzen tan trong brom tạo nên), lớp dưới là nước trong suốt.
Câu b: Khi cho brom lỏng vào ống nghiệm chứa benzene, lắc rồi để yên thì tạo thành dung dịch, màu brom sẽ nhạt đi do benzene tan trong brom lỏng.
Câu c: Cho thêm bột sắt vào ống nghiệm ở thí nghiệm b) rồi đun nhẹ thì hiện tượng quan sát được là: có khí thoát ra, màu brom nhạt dần. Do cấu tạo đặc biệt của benzen nên benzen chỉ tác dụng Br2 khan khi có xúc tác bột sắt. Khí thoát ra là HBr.
C6H6 + Br2 → C6H5Br + HBr (Fe, tº)
7. Giải bài 7 trang 192 SGK Hóa 11 nâng cao
Dùng công thức cấu tạo viết phương trình hóa học và gọi tên sản phẩm ở các phản ứng sau:
a) toluene + Cl2, có bột sắt
b) Toluen + Cl2, có chiếu sáng
c) Etylbenzen +HNO3, có mặt axit sunfuric đặc.
d) Etylbenzen +H2, có xúc tác Ni, đun nóng.
Phương pháp giải
- Do ảnh hưởng của nhân thơm đối với mạch nhánh, nên khi chiếu sáng toluene tham ra phản ứng thế nguyên tử hidro ở nhóm CH3.
- Quy tắc thế vào vòng benzen:
+ Nếu vòng benzen đã có sẵn nhóm thế loại I (-OH, ankyl, -NH2, …) thì phản ứng thế xảy ra dễ hơn so với benzen và ưu tiên thế vào vị trí o- và p-.
+ Nếu vòng benzen đã có sẵn nhóm thế loại II (-COOH, -CHO, -CH=CH2) thì phản ứng thế xảy ra khó hơn so với benzen và ưu tiên thế vào vị trí m-.
Hướng dẫn giải
Về nguyên tắc đề bài phải báo tỉ lệ mol, ở đây đề không báo nên giả sử tỉ lệ mol ở đây giữa toluene và Cl2 là 1: 1.
C6H5Cl + Cl2 → C6H4ClCH3 + HCl
C6H5CH3 + Cl2 → C6H5CH2Cl + HCl
C6H5C2H5 + HNO3 → C6H4NH2C2H5 + HCl
C6H5C2H5 + 3H2 → C6H11C2H5
8. Giải bài 8 trang 192 SGK Hóa 11 nâng cao
Hãy phân biệt 3 lọ hóa chất không nhãn chứa benzene, xiclohexan và xiclohexen.
Phương pháp giải
- Cho vào mỗi ống nghiệm 1 lượng dung dịch brom trong CCl4
- Tiếp tục cho vào 2 ống nghiệm còn lại 1 lượng HNO3/H2SO4 đặc
Hướng dẫn giải
Lấy vào mỗi ống nghiệm đã đánh số thứ tự tương ứng 1 lượng chất đã cho.
- Cho vào mỗi ống nghiệm 1 lượng dung dịch brom trong CCl4.
Ống nghiệm nào làm nhạt màu dung dịch brom là xilcohexen
- Tiếp tục cho vào 2 ống nghiệm còn lại 1 lượng HNO3/H2SO4 đặc.
Ống nghiệm nào tạo chất lỏng màu vàng là benzen
Mẫu còn lại là xiclohexan.
9. Giải bài 9 trang 192 SGK Hóa 11 nâng cao
Hidrocacbon C8H10 không làm mất màu nước brom, khi bị hidro hóa thì chuyển thành 1,4-đimetyl xiclohexan. Hãy xác định cấu tạo và gọi tên hidrocacbon đó theo 3 cách khác nhau.
Phương pháp giải
Gọi tên theo 3 cách 1,4-đimetyl benzene hoặc p-metyltoluen hoặc p-xilen
Hướng dẫn giải
C8H10 có k = 1/2 . (2.8+2-10)=4.
C8H10 không làm mất màu dung dịch brom.
⇒ C8H10 là hợp chất thơm, ngoài vòng benzene không có liên kết C = C.
C8H10 bị hidro hóa tạo ra 1,4-đimetyl xiclohexan.
Vậy công thức cấu tạo của C8H10 là CH3-C6H4-CH3
(1,4-đimetyl benzene hoặc p-metyltoluen hoặc p-xilen).
10. Giải bài 10 trang 192 SGK Hóa 11 nâng cao
Một học sinh lấy 100 ml benzene (D=0,879g|ml,20oC), brom lỏng (D = 3,1 g|ml,ở 20oC) và bột sắt để điều chế brombenzen.
a) Hãy vẽ dụng cụ đề thực hiện thí nghiệm đó (xem hình 7.3 và hình 8.1)
b) Tính thể tích brom cần dùng
c) Để hấp thụ khí sinh ra cần dùng dung dịch chứa tối thiểu bao nhiêu gam NaOH
d) Hãy đề nghị phương pháp tách lấy brombenzen từ hỗn hợp sau phản ứng, biết rằng nó là chất lỏng, sôi ở 156oC, D= 1,495 g/ml ở 20oC, tan trong benzene, không tan trong nước, không phản ứng với dung dịch kiềm.
e) Sau khi tinh chế, thu được 80 ml brombenzen (ở 20oC). Hãy tính hiệu suất phản ứng brom hóa benzene.
Phương pháp giải
- Viết phương trình hóa học của phản ứng
- Tính toán theo phương trình
Hướng dẫn giải
Câu a:
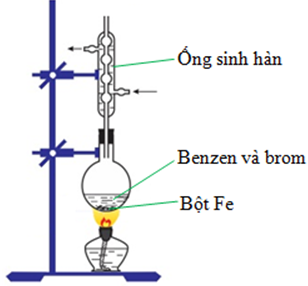
Câu b: mC6H6 = 0,879 . 1000 = 87,9 g ⇒ nC6H6 = 1,13 mol
C6H6 + Br2 → C6H5Br + HBr (1)
Từ (1) ⇒ nBr2 = 1,13 mol
⇒ VBr2 = 1,13.160/3,1 = 58,32(ml)
Câu c: Từ (1) ⇒ nHBr = nC6H6 = 1,13 mol
HBr + NaOH → NaBr + H2O (2)
1,13 mol
Từ (2) ⇒ nNaOH = 1,13 mol ⇒ mNaOH = 1,13 . 40 = 45,2 g
Câu d: Cho hỗn hợp sau phản ứng gồm C6H5Br, HBr, C6H6 dư và Br2 dư tác dụng với dung dịch NaOH loãng. HBr và Br2 tác dụng với NaOH, chiết thu được hỗn hợp gồm C6H5Br và C6H6 dư.
Chưng cất khoảng 80oC, C6H6 bay hơi thu được C6H5Br (C6H5Br có nhiệt độ sôi 156oC).
Câu e: Số mol C6H6 ban đầu là 1,13 mol
Khối lượng C6H5Br thực tế thu được.
mC6H5Br = V. D = 80 . 1,495 = 119,6 g ⇒ nC6H5Br = 0,76 mol
Từ (1) ⇒ Số mol C6H6 đã phản ứng là 0,76 mol
Hiệu suất phản ứng brom hóa benzene:
\(H\% = \frac{{0,76}}{{1,13}}.100\% = 67,26\% \)
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 47: Stiren và naphtalen
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 48: Nguồn hiđrocacbon thiên nhiên
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 49: Luyện tập: Hiđrocacbon thơm với hiđrocacbon no và không no