Giải bài tập SGK Hóa 11 Nâng cao Bài 48: Nguồn hiđrocacbon thiên nhiên
Dưới đây là Hướng dẫn giải Hóa 11 SGK nâng cao Chương 7 Bài 48 Nguồn hiđrocacbon thiên nhiên được eLib biên soạn và tổng hợp, nội dung bám sát theo chương trình SGK Hóa học 11 nâng cao giúp các em học sinh nắm vững phương pháp giải bài tập và ôn tập kiến thức hiệu quả hơn
Mục lục nội dung
1. Giải bài 1 trang 203 SGK Hóa học 11 nâng cao
2. Giải bài 2 trang 203 SGK Hóa học 11 nâng cao
3. Giải bài 3 trang 203 SGK Hóa học 11 nâng cao
4. Giải bài 4 trang 203 SGK Hóa học 11 nâng cao
5. Giải bài 5 trang 203 SGK Hóa học 11 nâng cao
6. Giải bài 6 trang 203 SGK Hóa học 11 nâng cao
7. Giải bài 7 trang 204 SGK Hóa học 11 nâng cao
8. Giải bài 8 trang 204 SGK Hóa học 11 nâng cao
9. Giải bài 9 trang 204 SGK Hóa học 11 nâng cao

1. Giải bài 1 trang 203 SGK Hóa 11 nâng cao
Hãy nêu tính chất vật lí, thành phần và tầm quan trọng của dầu mỏ.
Phương pháp giải
Để giải bài tập này các em cần nắm vững tính chất vật lí, thành phần...của dầu mỏ
Hướng dẫn giải
- Tính chất vật lí: Dầu mỏ là chất lòng sánh, màu nâu đen, không tan trong nước và nhẹ hơn nước.
- Thành phần của dầu mỏ: Dầu mỏ là một hỗn hợp phức tập gồm hàng trăm hidrocacbon thuộc các loại ankan, xicloankan, aren (hidrocacbon thơm). Ngoài ra, trong dầu mỏ còn có một lượng nhỏ các chất hữu cơ chứa oxi, nitơ, lưu huỳnh và vết các chất vô cơ.
- Vai trò của dầu mỏ: Dầu mỏ chủ yếu dùng để sản xuất dầu hỏa, diezen và xăng nhiên liệu. Ngoài ra, dầu thô cũng là nguồn nguyên liệu chủ yếu để sản xuất ra các sản phẩm của ngành hóa dầu như dung môi, phân bón hóa học, nhựa đường...
2. Giải bài 2 trang 203 SGK Hóa 11 nâng cao
Chọn câu đúng trong các câu sau:
A. Nhà máy “lọc dầu” là nhà máy chỉ lọc bỏ các tạp chất có trong dầu mỏ.
B. Nhà máy “lọc dầu” là nhà máy chỉ sản xuất xăng dầu.
C. Nhà máy “lọc dầu” là nhà máy chế biến dầu mỏ thành các sản phầm khác nhau.
D. Sản phẩm của nhà máy “lọc dầu” đều là các chất lỏng.
Phương pháp giải
Nhà máy “lọc dầu” là nhà máy chế biến dầu mỏ thành các sản phầm khác nhau.
Hướng dẫn giải
Chọn đáp án C.
Nhà máy “lọc dầu” là nhà máy chế biến dầu mỏ thành các sản phầm khác nhau.
3. Giải bài 3 trang 203 SGK Hóa 11 nâng cao
Hãy trình bày sơ lược về chưng cất dầu mỏ dưới áp suất thường (tên phân đoạn, số nguyên tử cacbon trong phân đoạn, ứng dụng của phân đoạn)
Phương pháp giải
- Dầu khai thác từ mỏ lên gọi là dầu thô.
- Dầu thô sau khi sơ chế loại bỏ nước, muối, được chưng cất ở áp suất thường trong các tháp chưng cất phân đoạn liên tục cao vài chục mét.
- Nhờ vậy, người ta tách được những phân đoạn dầu có nhiệt độ sôi khác nhau.
Hướng dẫn giải
Sơ đồ chưng cất dầu mỏ:
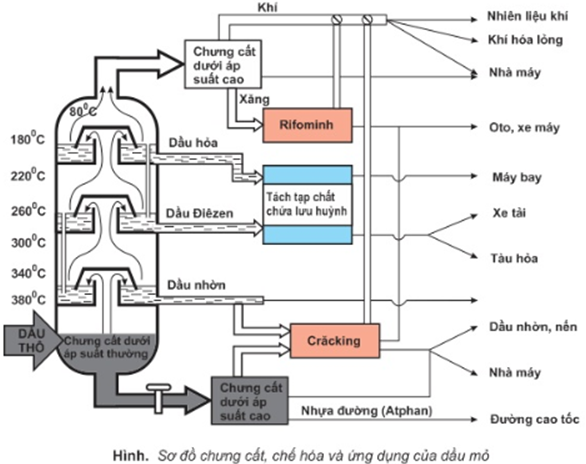
- Khi chưng cất dầu mỏ ở áp suất thường có các phân đoạn sau:
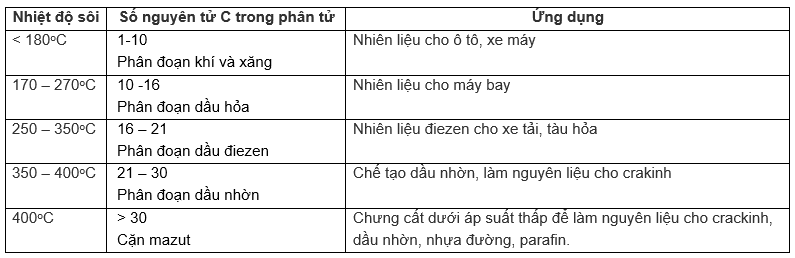
4. Giải bài 4 trang 203 SGK Hóa 11 nâng cao
Vì sao đối với phân đoạn sôi < 180oC cần phải chưng cất tiếp dưới áp suất cao, còn với phân đoạn sôi > 350oC cần phải chưng cất tiếp dưới áp suất thấp?
Phương pháp giải
Cần nắm vững các phương pháp chưng cất dầu mỏ
Hướng dẫn giải
- Đối với phân đoạn sôi < 180oC số nguyên tử C từ 1 - 4 là chủ yếu, tồn tại chủ yếu ở dạng khí dễ bay hơi nên phải chưng cất dưới áp suất cao mới tách được C1 - C2; C3 - C4.
- Đối với phân đoạn sôi > 350oC thành phần chủ yếu là cặn mazut có nhiệt độ sôi cao nên cần phải chưng cất dưới áp suất thấp.
5. Giải bài 5 trang 203 SGK Hóa 11 nâng cao
Rifominh là gì? Mục đích của rifominh? Cho thí dụ minh hoạ.
Phương pháp giải
- Rifominh là quá trình dùng xúc tác và nhiệt biến đổi cấu trúc của hidrocacbon
- Mục đích của rifominh là để tăng chỉ số octan
Hướng dẫn giải
Rifominh là quá trình dùng xúc tác và nhiệt biến đổi cấu trúc của hidrocacbon từ không phân nhánh thành phân nhánh, từ không thơm thành thơm.
Mục đích của rifominh là để tăng chỉ số octan
Ví dụ: Xăng được chưng cất từ dầu mỏ chứa chủ yếu là những ankan không phân nhánh vì vậy có chỉ số octan thấp, để tăng chỉ số octan người ta dùng phương pháp rifominh.
6. Giải bài 6 trang 203 SGK Hóa 11 nâng cao
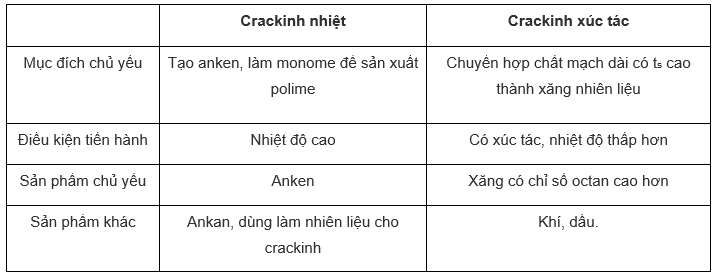
Hãy điền vào bảng so sánh crăckinh nhiệt và crăckinh xúc tác sau:
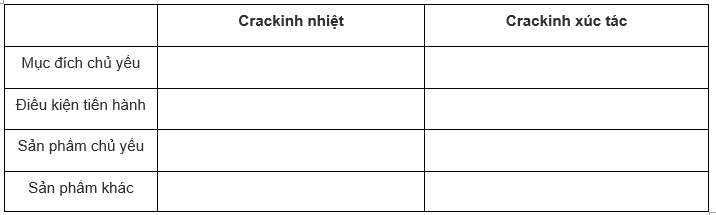
Phương pháp giải
- Crăkinh nhiệt thực hiện ở nhiệt độ trên 700−900oC chủ yếu tạo ra eten, propen, buten và penten dùng làm monome để sản xuất polime.
- Crăkinh xúc tác chủ yếu nhằm chuyển hiđrocacbon cacbon mạch dài của các phân đoạn có nhiệt độ sôi cao thành xăng nhiên liệu.
Hướng dẫn giải
7. Giải bài 7 trang 204 SGK Hóa 11 nâng cao
Dầu mỏ khai thác ở thềm lục địa phía Nam có đặc điểm là nhiều ankan mạch dài và hàm lượng S rất thấp. Các nhận định sau đúng hay sai:
a) Dễ vận chuyển theo đường ống.
b) Chưng cất phân đoạn sẽ thu được xăng chất lượng cao.
c) Crăckinh nhiệt sẽ thu được xăng với chất lượng cao.
d) Làm nguyên liệu cho crăckinh, rifominh tốt vì chứa ít S.
Phương pháp giải
Cần nắm được đặc điểm dầu mỏ ở thềm lục địa phía Nam
Hướng dẫn giải
- Nhận định đúng: d
- Nhận định sai: a, b, c
8. Giải bài 8 trang 204 SGK Hóa 11 nâng cao
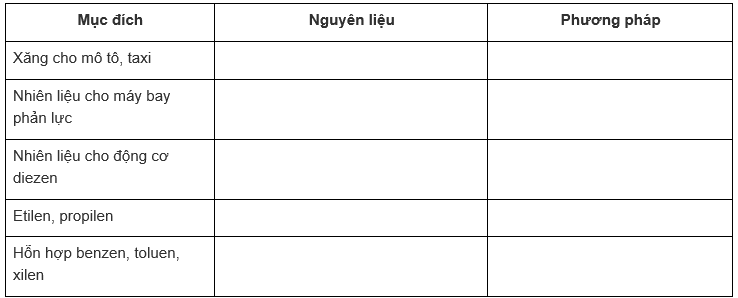
Hãy chọn nguyên liệu (phân đoạn nào, ts) và phương pháp (chưng cất, crăckinh nhiệt, crăckinh xúc tác) thích hợp cho các mục đích ghi trong bảng sau:
Phương pháp giải
Nắm đươc phương pháp và các giai đoạn chế biến dầu mỏ
Hướng dẫn giải
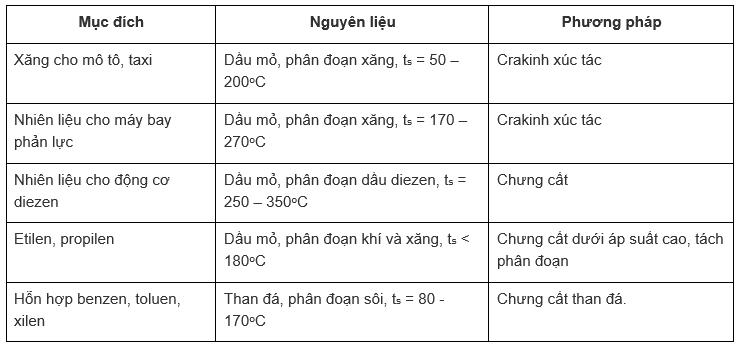
9. Giải bài 9 trang 204 SGK Hóa 11 nâng cao
a) Hãy nêu thành phần và ứng dụng của khí dầu mỏ, khí thiên nhiên, khí crăckinh và khí lò cốc.
b) Nhựa than đá là gì, có công dụng như thế nào?
Phương pháp giải
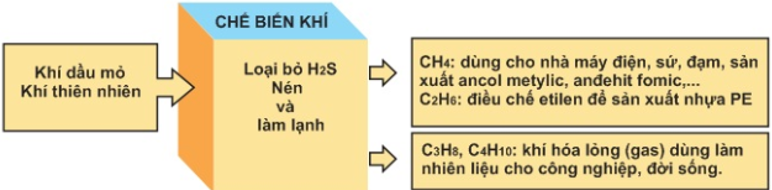
- Khí mỏ dầu còn gọi là khí đồng hành. Khí mỏ dầu có trong các mỏ dầu. Khí thiên nhiên là khí chứa trong các mỏ khí riêng biệt.
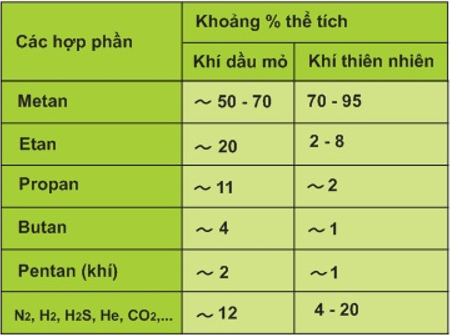
- Thành phần của khí mỏ dầu và khí thiên nhiên ở các mỏ khác nhau dao động như các số liệu ở bảng dưới đây:
Hướng dẫn giải
Câu a:
- Khí dầu mỏ: 51% CH4; 19% C2H6; 11% ; 4,4% C4H10; 2,1% C5H12 và 12,5% các khí khác (N2, H2, H2S, He....)
- Khí thiên nhiên: 92% CH4; 1,9% C2H6; 0,6% ; 0,3% C4H10; 1,1% C5H12 và 4,1% các khí khác (N2, H2, H2S, He....)
Ứng dụng của khí dầu mỏ và khí thiên nhiên:
+ CH4: dùng cho nhà máy điện, sứ, đạm, sản xuất ancol metylic
+ C2H6: Điều chế etilen sản xuất nhựa PE
+ C3H8, C4H10: Khí hóa lỏng dùng làm nhiên liệu cho công nghiệp, đời sống.
- Khí lò cốc: 65% H2; 35% CH4, CO2, CO, C2H6, N2.... dùng làm nhiên liệu.
- Khí crackinh là hỗn hợp khí chủ yếu của các hidrocacbon như CH4, C2H2, C3H6, .... phụ thuộc vào điều kiện phản ứng. Dùng làm nhiên liệu cho tổng hợp hữu cơ.
Câu b: Nhựa than đá là phần lỏng thu được khi chưng cất than đá. Lớp nhựa không tan trong nước tự tách ra. Ở mỗi phân đoạn thu được hợp chất:
- Dầu nhẹ: (80 - 170oC) chứa benzen, toluen, xilen....
- Dầu trung: (170 - 230oC) chứa naphtalen, phenol, piridin, ....
- Dầu nặng: (230 - 270oC) chứa crezol, xilenol,...
10. Giải bài 10 trang 204 SGK Hóa 11 nâng cao
Một loại xăng có thành phần về khối lượng như sau: hexan 43,0%, heptan 49,5%, pentan 1,80%, còn lại là octan. Hãy tính xem cần phải hỗn hợp 1,0g xăng đó tối thiểu với bao nhiêu lít không khí (đktc) để đảm bảo sự cháy được hoàn toàn và khi đó tạo ra bao nhiêu lít CO2.
Phương pháp giải
PTHH tổng quát:
\(\begin{array}{l}
{C_n}{H_{2n - 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\\
\to n{O_2} = \frac{{19}}{2}.\frac{{0,43}}{{86}} + 11.\frac{{0,495}}{{100}} + 8.\frac{{0,018}}{{72}} + \frac{{25}}{2}.\frac{{0,057}}{{114}} = 0,1102mol
\end{array}\)
⇒ Thể tích không khí tối thiểu cần dùng ?
nCO2 ⇒ VCO2 = ?
Hướng dẫn giải
1g xăng có:
mC6H4 = 0,43 g ⇒ nC6H4 = 0,43/86 mol
mC7H16 = 0,495 g ⇒ nC7H16 = 0,495/100 mol
mC5H12 = 0,018 g ⇒ nC5H12 = 0,018/72 mol
mC8H18 = 0,057 g ⇒ nC8H18 = 0,057/114 mol
PTHH tổng quát:
\(\begin{array}{l}
{C_n}{H_{2n - 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\\
\to n{O_2} = \frac{{19}}{2}.\frac{{0,43}}{{86}} + 11.\frac{{0,495}}{{100}} + 8.\frac{{0,018}}{{72}} + \frac{{25}}{2}.\frac{{0,057}}{{114}} = 0,1102mol
\end{array}\)
⇒ Thể tích không khí tối thiểu cần dùng là:
5. 0,1102 .22,4 = 12,325 lit
\(nCO_2 = 6.\frac{{0,43}}{{86}} + 7.\frac{{0,495}}{{100}} + 5.\frac{{0,018}}{{72}} + 8.\frac{{0,057}}{{114}} = 0,0699\)
VCO2 = 0,0699 . 22,4 = 1,566 lit
11. Giải bài 11 trang 204 SGK Hóa 11 nâng cao
Bảng dưới đây cho biết một số đặc tính hóa lí của 3 loại khí hóa lỏng thương phẩm (chứa tròn các bình GAS):
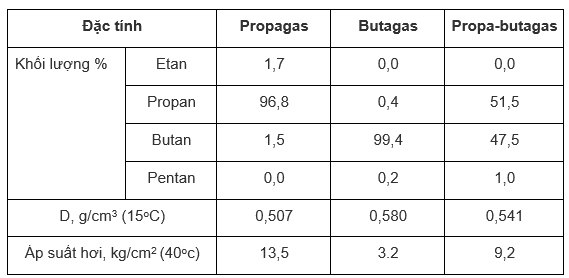
a) Hãy giải thích sự biến đổi khối lượng riêng, áp suất hơi từ loại *gas* này sang loại *gas* khác.
b) Hãy tính nhiệt tỏa ra khi đốt cháy hoàn toàn 1,0 kg mỗi loại *gas* kể trên và cho nhận xét. Biết rằng tỏa ra khi đốt cháy hoàn toàn 1 mol etan, propan, butan, pentan lần lượt bằng 1560, 2219, 2877, 3536 kJ.
c) Nhận xét khi đốt cháy hoàn toàn 1 mol metan, etilen, axetilen lần lượt bằng 890, 1410, 1300kJ. Vì sao người ta dùng axetilen làm nhiên liệu trong đèn xì mà không dùng etan, etilen hoặc metan ?
Phương pháp giải
- So sánh khối lượng riêng các chất
→ Nhiệt lượng tỏa ra khi đốt
Người ta dùng axetilen làm nhiên liệu trong đèn xì mà không dùng etan, etilen hoặc metan vì quá trình sản xuất axetilen từ CaC2 dễ dàng và tiện lợi hơn và axetilen cháy tỏa nhiều nhiệt.
Hướng dẫn giải
Câu a: Nhận thấy: Thành phần chính của 3 loại gas là propan và butan.
Propan có khối lượng riêng và nhiệt độ sôi đều nhỏ hơn butan nên propagas có khối lượng riêng nhỏ hơn nhưng áp suất hơi lớn hơn butagas. Còn gas hỗn hợp propa – butan gas có khối lượng riêng và áp suất hơi nằm trong khoảng giữa của 2 loại gas đó.
Câu b: 1kg propagas có:
17g C2H6; 968g C3H8; 1,5g C4H10
Nhiệt lượng tỏa ra khi đốt là:
\(\frac{{17}}{{30}}.1560 + \frac{{968}}{{44}}.2219 + \frac{{15}}{{58}}.2877 = 50446,05KJ\)
Làm tương tự ta được:
Nhiệt lượng tỏa ra khi đốt 1kg butagas là: 49605,78 kJ
Nhiệt lượng tỏa ra khi đốt 1kg propa- butagas là: 50025,14 kJ
Câu c: Người ta dùng axetilen làm nhiên liệu trong đèn xì mà không dùng etan, etilen hoặc metan vì quá trình sản xuất axetilen từ CaC2 dễ dàng và tiện lợi hơn và axetilen cháy tỏa nhiều nhiệt.
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 46: Benzen và ankylbenzen
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 47: Stiren và naphtalen
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 49: Luyện tập: Hiđrocacbon thơm với hiđrocacbon no và không no