Hoá học 11 Bài 25: Ankan
Nội dung bài Ankan tìm hiểu về Công thức chung của dãy đồng đẳng của ankan , CTCT, gọi tên của một số ankan đơn giản. Tính chất hoá học của ankan và phản ứng đặc trưng của RH no là phản ứng thế. Tầm quan trọng của RH no trong công nghiệp và trong đời sống. Từ đó hiểu Vì sao các ankan khá trơ về mặt hoá học , do đó hiểu được vì sao phản ứng đặc trưng là phản ứng thế.Vì sao các RH no lại được dùng làm nhiên liệu và nguyên liệu cho công nghiệp hoá chất, thấy được tầm quan trọng của RH no.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Đồng đẳng, đồng phân, danh pháp của Ankan
a. Đồng đẳng
Chất đầu tiên trong dãy ankan là metan: CH4, tiếp đến là C2H6, C3H8, C4H10....
Công thức chung CnH2n+2 (\(n \ge 1\))
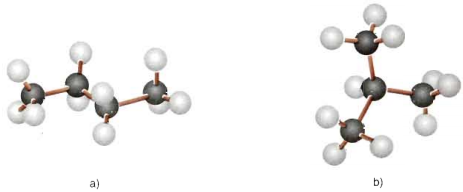
- Nhận xét về phân tử C4H10:
+ Chứa các liên kết đơn
+ Mỗi nguyên tử C tạo được 4 liên kết đơn hướng về 4 đỉnh của 1 hình tứ diện đều
+ Các nguyên tử C không nằm trên cùng 1 đường thẳng.
- Nhận xét chung về ankan:
+ Trong phân tử ankan chỉ có liên kết C-C và C-H
+ Mỗi nguyên tử Cacbon tạo được 4 liên kết đơn hướng từ nguyên tử C (nằm ở tâm hình tứ diện) về 4 đỉnh của hình tứ diện với góc liên kết \(\widehat {CCC},\widehat {HCH},\widehat {CCH}\) khoảng 109,5o
⇒ Các nguyên tử Cacbon trong phân tử ankan (trừ C2H6) không cùng nằm trên một đường thẳng.
b. Đồng phân
- Từ C4H10 trở đi có đồng phân cấu tạo (đồng phân mạch C).
- Bậc C: Bậc của nguyên tử C ở phân tử ankan bằng số nguyên tử C liên kết trực tiếp với nó.
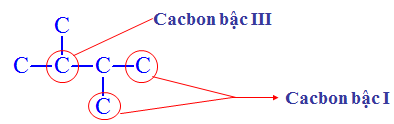
- Ankan chỉ chứa C bậc I và C bậc II là ankan không phân nhánh, chứa C bậc III và C bậc IV là ankan phân nhánh.
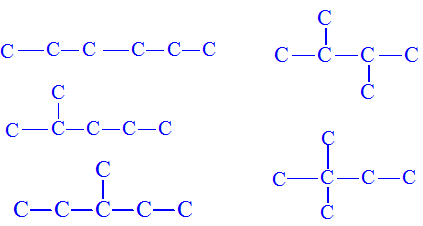
- Ví dụ 1: Viết đồng phân của C5H12
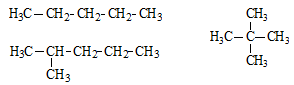
- Lưu ý: Nếu làm bài trắc nghiệm có thể đếm số đồng phân bằng cách:
+ Vẽ ra sườn cacbon, bỏ qua bước điền -H vì điều đó làm hình rối. Sau đó dùng mũi tên đánh dấu các vị trí nhánh là ta đếm đủ số đồng phân. Nhớ chú ý đến tính đối xứng của phân tử để tránh trùng lặp công thức.
+ Hoặc có thể sử dụng công thức tính số đồng phân của ankan là 2n-4 + 1 (với 3 < n < 7)
Ví dụ 2: Viết đồng phân của C6H14
Áp dụng công thức tính nhanh thì C6H14 có 2(6 - 4) + 1 = 5 đồng phân. thử kiểm tra lại bằng cách vẽ và đếm nhé!
c. Danh pháp
Tên hệ thống theo danh pháp IUPAC
a) Ankan không phân nhánh
Tên ankan = tên C mạch chính + an
Ví dụ: H3C-CH3 (etan); H3C-CH2-CH2-CH3 (Butan)
b) Ankan phân nhánh: Gọi theo kiểu tên thay thế.
Tên ankan = Số chỉ vị trí nhánh + Tên nhánh + Tên mạch chính + an
Tên gốc ankyl: Đổi đuôi an thành yl
CnH2n+2 → CnH2n+1
(ankan) (gốc ankyl)
Nhóm nguyên tử còn lại sau khi lấy bớt 1 nguyên tử H từ phân tử ankan, có công thức CnH2n+1, được gọi là nhóm ankyl. Tên của nhóm ankyl lấy từ tên của ankan tương ứng đổi đuôi an thành đuôi yl
Một số quy tắc gọi tên:
Mạch Cacbon chính là mạch C dài nhất.
Đánh số thứ tự các nguyên tử Cacbon mạch chính từ phía gần nhánh hơn.
Gọi tên nhánh theo thứ tự alphabe. Ví dụ: nhánh CH3- (metyl) với nhánh C2H5- (etyl) thì gọi tên nhánh etyl trước metyl vì chữ cái e đứng trước m trong thứ tự anphabe.
Nếu có nhiều nhánh giống nhau, ta thêm “đi” , “tri”, “tetra”, “penta”....
Lưu ý: không lấy kí tự đầu của từ chỉ số lượng nhánh để xét thứ tự gọi tên.
Ví dụ: (CH3)2- : Đimetyl ; C2H5- :Etyl
Tuyệt đối không lấy kí tự Đ trong từ chỉ số lượng "đi" để xét. Trong trường hợp này, ta dùng chữ cái đầu của tên nhánh là m và e, như vậy vẫn là gọi tên nhánh etyl trước, metyl sau.
Ví dụ 1: Gọi tên chất sau đây
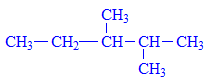
Có 2 cách đánh số mạch chính như sau:
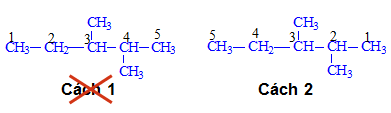
Cách 1: (Sai) vì hai nhánh có số là 3 và 4 thì sẽ lớn hơn Cách 2 (đúng) có số của hai nhánh là 2 và 3
Trong đó có chứa 2 nhánh CH3- (metyl) ta đọc tên là 2,3- Đimetylpentan
Ví dụ 2: Gọi tên chất sau đây
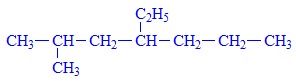
Ta đánh số thứ tự trước
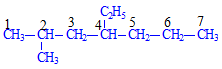
Trên đây có chứa 1 nhóm Etyl (C2H5-)và 1 nhóm mety (CH3-), vì chữ e đứng trước chữ m nên ta đọc nhánh etyl trước
Tên gọi: 4-etyl-2-metylheptan
1.2. Tính chất vật lý của Ankan
a. Nhiệt độ nóng chảy, nhiệt độ sôi, khối lượng riêng
Trạng thái: ở đk thường các ankan từ C1 → C4 ở trạng thái khí, từ C5 → C18 ở trạng thái lỏng, C19 trở đi ở trạng thái rắn.
t0nc, t0s của ankan nói chung đều tăng theo số nguyên tử C trong phân tử tức là tăng theo phân tử khối.
Khối lượng riêng tăng theo số nguyên tử C trong phân tử nhưng luôn nhỏ hơn khối lượng riêng của nước (ankan nhẹ hơn nước)
b. Tính tan
Không tan trong nước.
Là những dung môi không phân cực.
Hoà tan được vào những chất không phân cực. An kan lỏng có thể thấm qua da hoặc màng tế bào.
1.3. Tính chất hóa học của Ankan
Do chỉ có liên kết \(\delta \) tương đối bền vững, trơ về mặt hóa học, ở điều kiện thường chúng không phản ứng được với axit, bazo, các chất oxi hóa mạnh
Dưới tác dụng của nhiệt độ và ánh sáng ankan tham gia các phản ứng thế, phản ứng tách, phản ứng oxi hoá.
a. Phản ứng thế
CH4 + Cl2 → CH3Cl + HCl
clometan (metylclorua)
CH3Cl + Cl2 → CH2Cl2 + HCl
điclometan (metylenclorua)
CH2Cl2 + Cl2 → CHCl3 + HCl
triclometan (clorofom)
CHCl3 + Cl2 → CCl4 + HCl
tetraclometan (cacbontetra clorua)
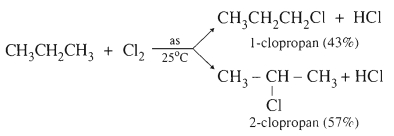
Nhận xét: Sản phẩm thế ưu tiên với H ở C bậc cao
b. Phản ứng tách
Gãy liên kết C-C, C-H; chất xúc tác thường dùng là Cr2O3, Fe, Pt.
- Tách H2 (Đề hidro hóa)
CH3-CH3 → CH2=CH2 + H2
- Phản ứng crackinh (bẻ gãy mạch cacbon)
C4H10 → (CH4 + CH3-CH=CH2) hoặc (C2H6 + CH2=CH2)
CH3-CH2-CH2-CH3 → (CH4 + C3H6) hoặc (C2H4 + C2H6) hoặc (C4H8 + H2)
c. Phản ứng Oxi hóa hoàn toàn
Phương trình phản ứng tổng quát đốt cháy:
CnH2n+2 + (3n+1)/2 O2 → nCO2 + (n + 1)H2O
⇒ số mol H2O luôn luôn lớn hơn CO2
Nếu thiếu Oxi, phản ứng cháy của ankan xảy ra không hoàn toàn, sản phẩm cháy ngoài CO2, H2O còn có CO, C ...
1.4. Điều chế Ankan
a. Phòng thí nghiệm
Làm thí nghiệm điều chế CH4 từ Natri axetat với vôi tôi xút.
CH3COONa+NaOH → CH4 +Na2CO3
Al4C3+12H2O → 3CH4 + 4Al(OH)3
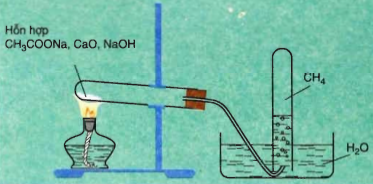
Hình 2: Điều chế Metan trong phòng thí nghiệm
Video: Điều chế Metan
b. Trong Công nghiệp
Metan và các đồng đẳng được tách từ khí thiên nhiên và dầu mỏ
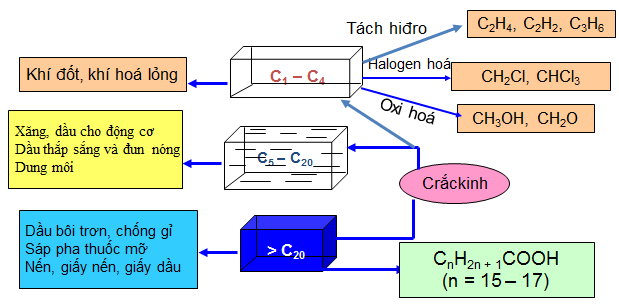
Hình 3: Metan và các đồng đẳng được tách từ khí thiên nhiên và dầu mỏ
1.5. Ứng dụng của Ankan
Từ C1 đến C20 được ứng dụng làm nhiên liệu
Nhiều Ankan được dùng làm dung môi và dầu bôi trơn máy.
Điều chế chất sinh hàn.
Nhờ tác dụng của nhiệt và các phản ứng oxy hoá không hoàn toàn → HCHO, rượu metylic , axitaxetic…v..v…
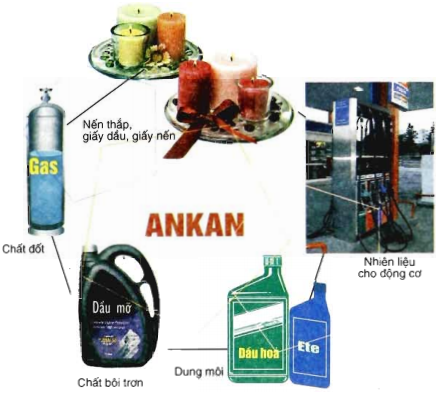
Hình 4: Ứng dụng của ankan
2. Bài tập minh họa
2.1. Dạng 1: Bài tập về đồng phân, gọi tên Ankan
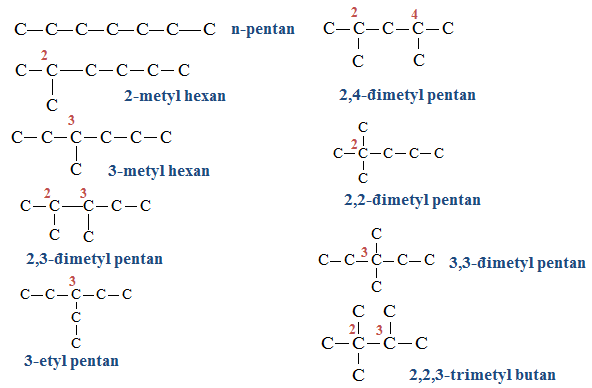
Viết và gọi tên các đồng phân của C7H16
Hướng dẫn giải
Áp dụng công thức tính nhanh số đồng phân có: 2(7-4) + 1 = 9 đồng phân
2.2. Dạng 2: Bài tập phản ứng oxi hóa ankan
Bài 1: Đốt cháy hoàn toàn 6,8g hỗn hợp khí X gồm: ankan A và CH4, sản phẩm cháy dẫn vào bình 1 đựng P2O5 và bình 2 đựng 1000 ml Ba(OH)2 0,5M. Sau thí nghiệm khối lượng bình 1 tăng 12,6g.
a. Tìm công thức phân tử của A, biết VA : VCH4 = 2 : 3.
b. Tính khối lượng các chất trong X.
c. Tính khối lượng muối tạo thành.
Hướng dẫn giải
VA : VCH4 = 2 : 3 ⇒ nA : nCH4 = 2x : 3x
Khối lượng bình 1 tăng là khối lượng của H2O: nH2O = 12,6/18 = 0,7 mol
a. Gọi CTPT của ankan là CnH2n+2
CnH2n+2 + (3n+1)/2 O2 → nCO2 + (n + 1)H2O
2x (n+1),2x
CH4 + 2O2 → CO2 + 2H2O
3x 6x
Ta có: (14n + 2).2x + 16.3x = 6,8 (1) ; (n + 1).2x + 6x = 0,7(2)
Từ 1, 2 ⇒ x = 0,05 và nx = 0,15 ⇒ n = 3
Vậy CTPT của A là C3H8
b. Khối lượng của mỗi an kan trong hỗn hợp X là
mC3H8 = 2.0,05.44 = 4,4 gam ⇒ mCH4 = 6,8 – 4,4 = 2,4 gam
c. Số mol CO2 tạo thành là nCO2 = 2.0,15 + 3.0,05 = 0,45 mol
Số mol Ba(OH)2 là: nBa(OH)2 = 1.0,5 = 0,5 mol
\(T = \frac{{nO{H^ - }}}{{nC{O_2}}} = \frac{{2.0,5}}{{0,45}} = 2,22\) ⇒ chỉ tạo muối BaCO3
Khối lượng muối tạo thành: mBaCO3 = 0,45.197 = 88,65 gam
2.3. Dạng 3: Bài tập phản ứng đề hidro hóa và cracking ankan
Bài 1: Crackinh butan thu được 35 mol hh A gồm CH4, C2H6, H2, C2H4, C3H6, C4H8 và C4H10 dư. Dẫn A lội qua bình nước brom dư thấy có 20 mol khí đi ra khỏi bình (biết rằng chỉ có C2H4, C3H6, C4H8 phản ứng với Br2 và đều theo tỉ lệ số mol 1:1). Nếu đốt cháy hoàn toàn A thì thu được a mol CO2.
a. Tính hiệu suất phản ứng tạo hh A.
b. Tính giá trị của a.
Hướng dẫn giải
a. Phương trình phản ứng:
C4H10 → CH4 + C3H6
C4H10 → C2H6 + C2H4
C4H10 → H2 + C4H8
Số mol anken thu được: nanken= 35 - 20 = 15mol
Số mol butan ban đầu là: nđ = nbutan = ns - nanken = 35 – 15 = 20 mol
Hiệu suất cracking butan là H = (ns- nđ)/nđ .100% = (35-20)/20.100% = 75%
b. Đốt cháy hỗn hợp A là đốt chay butan:
C4H10 + 11/2O2 → 4CO2 + 5H2O
20 80 mol
Vậy số mol CO2 thu được khi đốt cháy hỗn hợp A là 80 mol
2.4. Dạng 4: Bài tập phản ứng halogen hóa Ankan
Bài 1: Một ankan A có thành phần phần trăm C là 83,33%. Tìm CTPT và xác định CTCT đúng của A biết rằng khi cho A tác dụng với Cl2 theo tỉ lệ mol 1: 1 ta chỉ thu được 1 sản phẩm thế monoclo.
Hướng dẫn giải
Gọi CTPT của ankan là: CnH2n+2
%(m)C = 12n/(12n+2n+2).100% = 83,33%
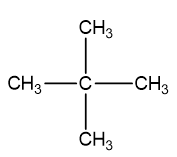
⇒ n = 5. Vậy CTPT của A là C5H12
A tác dụng với Cl2 theo tỉ lệ mol 1: 1 ta chỉ thu được 1 sản phẩm thế monoclo.
⇒ CTCT đúng của A là:
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Cho m metan tác dụng vừa đủ với Br2 vừa đủ chỉ thu được 2 sản phẩm gồm 37,95 gam dẫn xuất X và 36,45 gam chất vô cơ Y. Giá trị của m là?
Câu 2: Craking m gam n-butan thu được hợp A gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và một phần butan chưa bị craking. Đốt cháy hoàn toàn A thu được 9 gam H2O và 17,6 gam CO2. Giá trị của m là?
Câu 3: Đốt cháy hoàn toàn một lượng hi đrocacbon X. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ba(OH)2 (dư) tạo ra 29,55 gam kết tủa, dung dịch sau phản ứng có khối lượng giảm 19,35 gam so với dung dịch Ba(OH)2 ban đầu. Công thức phân tử X là?
Câu 4: Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. thể tích không khí (dktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên niên trên là
Câu 5: Đốt cháy hết 2,24 lít ankan X (đktc), dẫn toàn bộ sản phẩm cháy vào dd nước vôi trong dư thấy có 40g kết tủa. CTPT X
3.2. Bài tập trắc nghiệm
Câu 1: Ankan X có công thức phân tử C5H12. Clo hóa X, thu được 4 sản phẩm dẫn xuất monoClo. Tên gọi của X là
A. 2,2-đimetylprotan
B. 2- metylbutan
C. pentan
D. 2- đimetylpropan
Câu 2: Cho 2-metylbutan tác dụng với Cl2 (ánh sáng, tỉ lệ số mol 1 : 1), số sản phẩm monoClo tối đa thu được là
A. 2
B. 3
C. 5
D. 4.
Câu 3: Khi crackinh hoàn toàn một thể tích ankan X thu được ba thể tích hỗn hợp Y (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 12. Công thức phân tử của X là:
A. C6H14.
B. C3H8.
C. C4H10.
D. C5H12.
Câu 4: Khi đốt cháy hoàn toàn 7,84 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được 16,8 lít khí CO2 (đktc) và x gam H2O. Giá trị của x là
A. 6,3.
B. 13,5.
C. 18,0.
D. 19,8.
Câu 5: Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X tác dụng với khí Clo (theo tỉ lệ số mol 1 : 1) thu được một sản phẩm hữu cơ duy nhất . Tên gọi của X là
A. 2,2-đimetylpropan
B. etan
C. 2-metylpropan
D. 2- metylbutan
3.3. Trắc nghiệm Online
Các em hãy luyện tập bài trắc nghiệm Ankan Hóa học 11 sau để nắm rõ thêm kiến thức bài học.
4. Kết luận
Sau bài học cần nắm:
- Lập dãy đồng đẳng , viết các đồng phân.
- Viết và xác định được các sản phẩm chính của phản ứng thế, gọi được tên các ankan cũng như các sản phẩm tạo ra trong các phản ứng đó.
Tham khảo thêm
- doc Hoá học 11 Bài 26: Xicloankan
- doc Hoá học 11 Bài 27: Luyện tập Ankan và xicloankan
- doc Hoá học 11 Bài 28: Bài thực hành số 3 Phân tích định tính nguyên tố và Điều chế và tính chất của metan