Giải bài tập SGK Hóa 10 Nâng cao Bài 26: Phân loại phản ứng trong hóa học vô cơ
Dưới đây là Hướng dẫn giải Hóa 10 SGK nâng cao Chương 4 Bài 26 Phân loại phản ứng trong hóa học vô cơ được eLib biên soạn và tổng hợp, nội dung bám sát theo chương trình SGK Hóa học 10 nâng cao giúp các em học sinh nắm vững phương pháp giải bài tập và ôn tập kiến thức hiệu quả hơn.
Mục lục nội dung
1. Giải bài 1 trang 109 SGK Hóa học 10 nâng cao
2. Giải bài 2 trang 109 SGK Hóa học 10 nâng cao
3. Giải bài 3 trang 110 SGK Hóa học 10 nâng cao
4. Giải bài 4 trang 110 SGK Hóa học 10 nâng cao
5. Giải bài 5 trang 110 SGK Hóa học 10 nâng cao
6. Giải bài 6 trang 110 SGK Hóa học 10 nâng cao

1. Giải bài 1 trang 109 SGK Hóa 10 nâng cao
Trong các phản ứng hóa hợp dưới đây, phản ứng nào là phản ứng oxi hóa – khử?
A. CaCO3 + H2O + CO3 → Ca(HCO3)2
B. P2O5 + 3H2O → 2H3PO4
C. 2SO2 + O2 → 2SO3
D. BaO + H2O → Ba(OH)2
Phương pháp giải
Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron giữa các chất trong phản ứng hay phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số nguyên tố.
Hướng dẫn giải
Chọn C.
Phản ứng: 2SO2 + O2 → 2SO3 : Là phản ứng oxi hóa khử vì có sự thay đổi số oxi hóa của các nguyên tố
2. Giải bài 2 trang 109 SGK Hóa 10 nâng cao
Trong các phản ứng phân hủy dưới đây, phản ứng nào không phải là phản ứng oxi hóa – khử?
A. 2KMnO4 → K2MnO2 + MnO2 + O2
B. 2Fe(OH)3 → Fe2O3 + 3H2O
C. 4KClO3 → 3KClO4 + KCl
D. 2KClO3 → 2KCl + 3O2
Phương pháp giải
Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron giữa các chất trong phản ứng hay phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số nguyên tố.
Hướng dẫn giải
2Fe(OH)3 → Fe2O3 + 3H2O
→ Đáp án cần chọn là B.
3. Giải bài 3 trang 110 SGK Hóa 10 nâng cao

Hãy điển các ví dụ vào ô trống, mỗi ô ghi lại 2 phương trình hóa học (nếu có) không trùng với các phản ứng trong Giải bài học, có ghi rõ số oxi hóa của các nguyên tố. Để trống các ô không phản ứng thích hợp.
Phương pháp giải
- Phản ứng hoá hợp : Là phản ứng hóa học, trong đó 2 hay nhiều chất hóa hợp với nhau tạo thành một chất mới.
- Phản ứng phân huỷ: Là phản ứng hóa học, trong đó một chất bị phân hủy thành 2 hay nhiều chất mới
- Phản ứng thế: Là phản ứng hóa học, trong đó nguyên tử của nguyên tố này ở dạng đơn chất thay thế nguyên tử của nguyên tố khác trong hợp chất
- Phản ứng trao đổi : Là phản ứng hóa học, trong đó các hợp chất trao đổi nguyên tử hay nhóm nguyên tử với nhau
Hướng dẫn giải
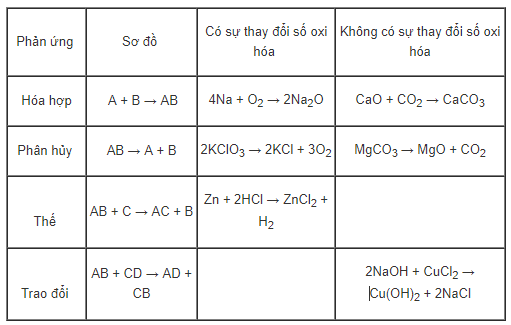
4. Giải bài 4 trang 110 SGK Hóa 10 nâng cao
Người ta có thể tổng hợp được amoniac (NH3) từ khí nitơ và khí hiđro.
a) Viết phương trình hóa học.
b) Số oxi hóa của các nguyên tố biến đổi như thế nào trong phản ứng hóa học đó?
Phương pháp giải
- Viết PTHH của phản ứng → xác định số oxi hóa từng chất
Hướng dẫn giải
Câu a: Phản ứng xảy ra: N2 + 3H2 → 2NH3
Câu b: Nitơ có số oxi hóa giảm từ 0 xuống -3. Còn hiđro có số oxi hóa tăng từ 0 lên +1.
5. Giải bài 5 trang 110 SGK Hóa 10 nâng cao
a) Viết phương trình hóa học của những biến đổi sau:
- Sản xuất vôi sống bằng cách nung đá vôi.
- Cho vôi sống tác dụng với nước (tôi vôi).
b) Số oxi hóa của các nguyên tố trong những phản ứng trên có biến đổi không?
Phương pháp giải
- Viết PTHH của phản ứng → xác định số oxi hóa từng chất
Hướng dẫn giải
Câu a: Các phản ứng hóa học:
- Phản ứng sản xuất vôi: CaCO3 (1000oC) → CaO + CO2
- Phản ứng tôi vôi: CaO + H2O → Ca(OH)2
Câu b: Trong các phản ứng trên không có sự thay đổi số oxi hóa.
6. Giải bài 6 trang 110 SGK Hóa 10 nâng cao
Glixerol trinitrat là chất nổ đinamit. Đó là một chất lỏng có công thức phân tử C3H5O9N3, rất không bền, bị phân hủy tạo ra CO2, H2O, N2 và O2.
a) Viết phương trình hóa học của các phản ứng phân hủy glixerol trinitrat.
b) Hãy lính thể tích khí sinh ra khi làm nổ 1 kg chất nổ này. Biết rằng ở điều kiện phản ứng, 1 mol khí có thể tích là 50 lít.
Phương pháp giải
4C3H5O9N3 → 12CO2 + 10H2O + 6N2 + O2
nglixerol = ?
Cứ 4 mol glixerol trinitrat khi nổ tạo ra 29 mol chất khí vậy 1kg glixerol trinitrat khi nổ tạo ra số mol chất khí?
Hướng dẫn giải
Câu a: Phương trình phản ứng:
4C3H5O9N3 → 12CO2 + 10H2O + 6N2 + O2
Câu b: nglixerol = 1000/227 mol
Thể tích khí sinh ra:
Theo phản ứng: Cứ 4 mol glixerol trinitrat khi nổ tạo ra 29 mol chất khí
Vậy 1kg glixerol trinitrat khi nổ tạo ra số mol chất khí:
⇒ n = (29.1000)/(4.227) = 31,94(mol) ⇒ Vkhí = 31,94 x 50 ≈ 1597 (lít).
7. Giải bài 7 trang 110 SGK Hóa 10 nâng cao
Hợp chất A (không chứa clo) cháy được trong khí clo tạo ra nitơ và hiđro clorua.
a) Xác định công thức phân tử của khí A, biết rằng tỉ lệ giữa thể tích khí clo tham gia phản ứng và thể tích nitơ tạo thành là 3: 1.
b) Viết phương trình hóa học của phản ứng giữa A và clo.
c) Tính số oxi hóa của tất cả các nguyên tố trước và sau phản ứng.
Phương pháp giải
A + Cl2 → N2 + 2HCl
VCl2 : VN2 ⇒ VHCl : VN2
→ Công thức phân tử của A
Hướng dẫn giải
Câu a: Xác định công thức khí A:
Sơ đồ phản ứng: A + Cl2 → N2 + 2HCl
Theo sơ đồ ta thấy: Cứ 1 thể tích Clo tương ứng tạo ra 2 thể tích khí HCl
Từ tỉ lệ: VCl2 : VN2 = 3:1 ⇒ VHCl : VN2 = 6:1
Vậy trong phân tử A có 3 nguyên tố H và 1 nguyên tử N. Công thức phân tử của A là: NH3.
Câu b: Phản ứng: 2NH3 + 3Cl2 → N2 + 6HCl
Câu c: Tính số oxi hóa:
N+3 → N2o
Cl2o → Cl-
8. Giải bài 8 trang 110 SGK Hóa 10 nâng cao
Cho ba ví dụ về phản ứng tỏa nhiệt và ba ví dụ về phản ứng thu nhiệt.
Phương pháp giải
Phản ứng tỏa nhiệt là phản ứng hóa học giải phóng năng lượng dưới dạng nhiệt. Phản ứng tỏa nhiệt thì các chất phản ứng phải mất bớt năng lượng, vì thế ΔH có giá trị âm
Phản ứng thu nhiệt là phản ứng hóa học hấp thu năng lượng dưới dạng nhiệt. Phản ứng thu nhiệt thì các chất phản ứng phải tăng thêm năng lượng, vì thế ΔH có giá trị dương
Hướng dẫn giải
Ba ví dụ về phản ứng tỏa nhiệt (ΔH < 0):
C(r) +O2(k) → CO2(k) (ΔH = -393,5 KJ/mol)
CuSO4(dd) + Zn(r) → ZnSO4(dd) + Cu(r); ΔH = -231,04 KJ/mol
HI(k) → 1/2H2(k) + 1/2I2(k) ; ΔH = -25,9 KJ/mol
Ba ví dụ về phản ứng thu nhiệt (ΔH > 0):
C(r) + H2O(k) → CO(k) + H2(k); ΔH = + 131,25 KJ/mol
1/2H2(k) + 1/2I2(k) → HI(k); ΔH = + 25,9 KJ/mol
CaCO3(r) → CaO(r) + CO2(k); ΔH =+ 177,9 KJ/mol
Tham khảo thêm
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 25: Phản ứng oxi hóa khử
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 27: Luyện tập Chương 4