Hóa học 9 Bài 20: Hợp kim sắt: Gang, thép
Trong đời sống và trong kĩ thuật hợp kim của sắt là gang, thép được sử dụng rất rộng rãi. Thế nào là gang, thép? Gang thép được sản xuất như thế nào? Hôm nay các em sẽ được nghiên cứu.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Hợp kim của sắt
- Hợp kim là chất rắn thu được sau khi làm nguội hỗn hợp nóng chảy của nhiều kim loại khác nhau hoặc của kim loại và phi kim.
- Hợp kim của sắt có nhiều ứng dụng là gang và thép.
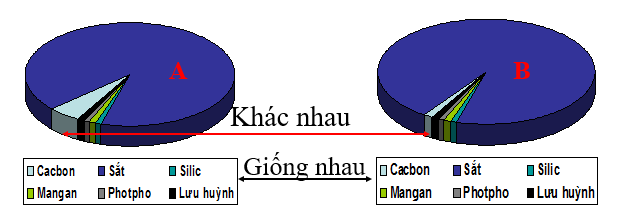
A- Thành phần của Gang, B-Thành phần của Thép
a. Gang là gì?
- Gang là hợp kim của sắt với một số nguyên tố khác (C, Mn, S, Si,…) . Trong đó hàm lượng Cacbon chiếm từ 2-5%.
- Đặc điểm: Gang cứng và giòn.
- Ứng dụng:
- Gang trắng dùng để luyện thép...
- Gang xám dùng để đúc máy, ống dẫn nước...
b. Thép là gì?
- Thép là hợp kim của sắt với một số nguyên tố khác (C, Mn, S, Si,…) . Trong đó hàm lượng Cacbon chiếm dưới 2%.
- Đặc điểm: Thép thường cứng, đàn hồi, ít bị ăn mòn,…
- Ứng dụng:
- Dùng để chế tạo các chi tiết máy, vật dụng, dụng cụ lao động…
- Dùng làm vật liệu xây dựng, chế tạo phương tiện giao thông, vận tải,…
1.2. Sản xuất Gang, Thép
a. Sản xuất Gang như thế nào?
- Nguyên liệu sản xuất Gang

-
Quặng sắt : Hematit (chứa Fe2O3), manhetit (chứa Fe3O4)
-
Than cốc, không khí giàu khí ôxi, phụ gia (CaCO3,…)
- Nguyên tắc sản xuất gang
- Dùng Cacbon oxit khử oxit sắt ở nhiệt độ cao trong lò luyện kim
- Các phản ứng xảy ra trong lò gang
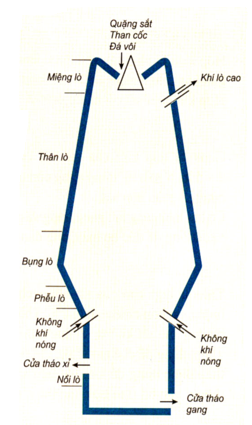
-
Phương trình:
C(r) + O2 (k) .PNG)
CO2 (k) + C(r) .PNG)
-
Khí CO khử oxit trong quặng thành sắt:
Fe2O3(r) + 3CO(k) → 2Fe(r) + 3CO2 (k)
- Sắt nóng chảy hòa tan một lượng nhỏ cacbon và các nguyên tố khác thành gang lỏng chảy xuống nồi lò và được đưa ra ngoài ra cửa tháo gang.
-
Đá vôi bị phân hủy tạo thành CaO. CaO kết hợp với các oxit SiO2 tạo thành xỉ
CaO(r) + SiO2(r) → CaSiO3 (r)
b. Sản xuất Thép như thế nào?
- Nguyên liệu sản xuất thép
- Gang, sắt phế liệu và khí ôxi.
- Nguyên tắc sản xuất thép
- Oxi hoá kim loại, phi kim để loại các nguyên tố cacbon, silic, mangan,…ra khỏi gang
- Quá trình sản xuất thép
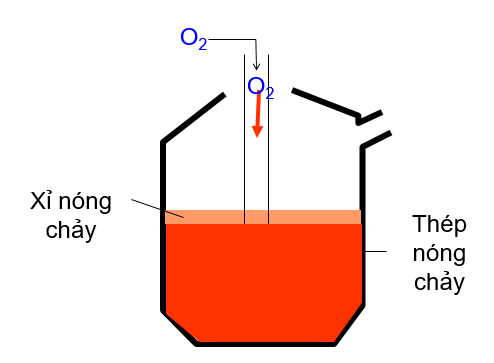
- Các phản ứng xảy ra trong quá trình sản xuất thép
- Thổi khí ôxi vào lò đựng gang và sắt nóng chảy ở nhiệt độ cao . Khí ôxi oxi hoá sắt thành oxit sắt FeO . Sau đó FeO sẽ oxi hoá một số nguyên tố trong gang như C, Mn, Si, S, P,…
- Các phương trình phản ứng:
Fe(r) + O2 (k) .PNG)
FeO (r) + C (r) .PNG)
FeO (r) + Mn (r) .PNG)
FeO (r) + Si (r) .PNG)
2. Bài tập minh họa
2.1. Dạng 1: Bài toán về luyện gang, thép
Dùng 100 tấn quặng Fe3O4 để luyện gang (95% sắt). Tính khối lượng gang thu được. Cho biết hàm lượng Fe3O4 trong quặng là 80%. Hiệu suất quá trình phản ứng là 93%.
Hướng dẫn giải
Khối lượng Fe3O4:
100 . 80 / 100 = 80 tấn
Trong 232 tấn Fe3O4 có 168 tấn Fe
80 tấn Fe3O4 có y tấn Fe
→ y = 57,931 (tấn)
Khối lượng Fe để luyện gang:
57,931 . 93/100 = 53,876 tấn
Khối lượng gang thu được:
53,876 .100 / 95 = 56,712 tấn
Vậy khối lượng gang thu được là 56,712 tấn.
2.2. Dạng 2: Phương trình luyện gang, thép
Hãy lập các phương trình hoá học theo sơ đồ sau đây:
a) O2 + 2Mn \(\xrightarrow{{{t^o}}}\) 2MnO
b) Fe2O3 + CO \(\xrightarrow{{{t^o}}}\) Fe + CO2
c) O2 + Si \(\xrightarrow{{{t^o}}}\) SiO2
d) O2 + S \(\xrightarrow{{{t^o}}}\) SO2
Cho biết phản ứng nào xảy ra trong quá trình luyện gang, phản ứng nào xảy ra trong quá trình luyện thép, chất nào là chất oxi hoá, chất nào là chất khử?
Hướng dẫn giải
Phương trình hóa học theo sơ đồ trên:
a) O2 + 2Mn \(\xrightarrow{{{t^o}}}\) 2MnO
b) Fe2O3 + 3CO \(\xrightarrow{{{t^o}}}\) 2Fe + 3CO2
c) O2 + Si \(\xrightarrow{{{t^o}}}\) SiO2
d) O2 + S \(\xrightarrow{{{t^o}}}\) SO2
- Phản ứng xảy ra trong quá trình luyện gang là (b).
- Phản ứng xảy ra trong luyện thép là (a), (c), (d).
- Chất oxi hóa là O2, Fe2O3.
- Chất khử là Mn, CO, Si, S.
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Tính khối lượng quặng hematit chứa 60% Fe2O3 cần thiết để sản xuất được 1 tấn gang chứa 95% Fe. Biết hiệu suất của quá trình là 80%?
Câu 2: Cứ 1 tấn quặng FeCO3 hàm lượng 80% đem luyện thành gang (95% sắt) thì thu được 378 kg gang thành phẩm. Tính hiệu suất của quá trình phản ứng.
Câu 3: Để có 1 tấn thép (98% Fe) cần dùng bao nhiêu tấn quặng hematit nâu (Fe2O3.2H2O) ? Hàm lượng hematit nâu trong quặng là 80%. Hiệu suất quá trình phản ứng là 93%.
3.2. Bài tập trắc nghiệm
Câu 1: Từ 1,2 tấn quặng Hematit (có chứa 85% oxit sắt) có thể sản xuất được …………… Gang (có chứa 95% Fe).
A. 0,52 tấn.
B. 0,62 tấn.
C. 0,75 tấn.
D. 0,72 tấn.
Câu 2: Sơ đồ nào sau đây biểu diễn quá trình luyện gang từ quặng sắt:
A. FeO ---> Fe3O4 ---> Fe
B. Fe2O3 ---> FeO ---> Fe
C. Fe2O3 ---> FeO ---> Fe
D. Fe2O3 ---> Fe3O4 ---> FeO ---> Fe
Câu 3: Nguyên liệu dùng để sản xuất thép là:
A. Gang , sắt phế liệu
B. Quặng sắt
C. Cacbon , silic , mangan
D. Cả A ,B và C
Câu 4: Nguyên tắc sản xuất thép là:
A. O2 + 2 Fe → 2FeO
B. C + O2 → CO2
C. FeO + C → Fe + CO
D. Fe + Mn → Fe + MnO
4. Kết luận
Sau bài học cần nắm:
- Khai thác thông tin về sản xuất gang thép từ sơ đồ lò luyện gang và lò luyện thép.
- Viết được các PTHH chính xảy ra trong quá trình sản xuất gang và quá trình sản xuất thép.
- Áp dụng vào các bài tập liên quan, hiệu suất luyện gang thép.
Tham khảo thêm
- docx Hóa học 9 Bài 15: Tính chất vật lí của kim loại
- docx Hóa học 9 Bài 16: Tính chất hóa học của kim loại
- doc Hóa học Bài 17: Dãy hoạt động hóa học của kim loại
- docx Hóa học 9 Bài 18: Nhôm
- doc Hóa học 9 Bài 19: Sắt
- doc Hóa học 9 Bài 21: Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn
- doc Hóa học 9 Bài 22: Luyện tập chương 2 Kim loại
- doc Hoá học 9 Bài 23: Thực hành: Tính chất hóa học của nhôm và sắt
- doc Hóa học 9 Bài 24: Ôn tập học kì 1