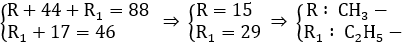Giải bài tập SGK Hóa 12 Bài 4: Luyện tập Este và chất béo
Nội dung hướng dẫn Giải bài tập Hóa 12 Bài 4 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 18 SGK Hóa 12
So sánh chất béo và este về: Thành phần nguyên tố, đặc điểm cấu tạo phân tử và tính chất hóa học.
Phương pháp giải
Để so sánh chất béo và este cần nắm được khái niệm, đặc điểm cấu tạo và tính chất hóa học của este và chất béo.
Hướng dẫn giải
- Thành phần nguyên tố: Đều chứa: C, H, O
- Đặc điểm cấu tạo:
- Este: Trong phân tử este của axit cacboxylic có nhóm -COOR với gốc hiđrocacbon
- Chất béo: Là trieste của axit béo có mạch cacbon dài với glixerol
- Tính chất hóa học: Đều có các phản ứng sau:
- Phản ứng thủy phân trong môi trường axit:
RCOOR' + H2O ⇔ RCOOH + R'OH
- Phản ứng xà phòng hóa:
RCOOR' + NaOH → RCOONa + R'OH
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
- Phản ứng hirđro hóa chất béo lỏng
- Tính chất vật lý: Este và chất béo đều nhẹ hơn nước, không tan trong nước nhưng tan nhiều trong các dung môi hữu cơ
2. Giải bài 2 trang 18 SGK Hóa 12
Khi đun hỗn hợp 2 axit cacboxylic với glixerol (axit H2SO4 làm xúc tác) có thể thu được mấy trieste ? Viết công thức cấu tạo của các chất này.
Phương pháp giải
Để viết công thức cấu tạo của trieste, ta cần thực hiện các bước sau:
- Bước 1: Viết công thức chung của este dạng (R1COO)xC3H5(R2COO)y với x + y = 3.
- Bước 2: Xét các trường hợp tương ứng với xác giá trị x, y → công thức cấu tạo.
Hướng dẫn giải
Các este thu được, khi đun hỗn hợp 2 axit cacboxylic với glixerol (axit H2SO4 làm xúc tác):
Giả sử 2 axit là R1COOH và R2COOH
Các trieste sẽ có dạng (R1COO)xC3H5(R2COO)y với x + y = 3
- Trường hợp 1:
Với x = 3, y = 0 thì ta thu được 1 trieste như sau:
- Trường hợp 2:
Với x = 0, y = 3 thì ta thu được 1 trieste như sau:
- Trường hợp 3:
Với x = 2, y = 1 thì ta thu được 2 trieste như sau:
- Trường hợp 4:
Với x = 1, y = 2 thì ta thu được 2 trieste như sau:
Vậy khi đun hỗn hợp 2 axit cacboxylic với glixerol (axit H2SO4 làm xúc tác) có thể thu được 6 trieste có công thức cấu tạo như trên.
3. Giải bài 3 trang 18 SGK Hóa 12
Khi thủy phân (xúc tác axit) một este thu được glixerol và hỗn hợp axit stearic (C17H35COOH) và axit panmitic (C15H31COOH) theo tỉ lệ 2 : 1.
Este có thể có công thức cấu tạo nào sau đây?
Phương pháp giải
Để xác định công thức cấu tạo của este, ta dựa vào tỉ lệ của 2 axit tạo thành este đó.
Hướng dẫn giải
Hỗn hợp axit stearic (C17H35COOH) và axit panmitic (C15H31COOH) theo tỉ lệ 2 : 1 nên este có 2 gốc C17H35COO và 1 gốc C15H31COO
→ Đáp án B
4. Giải bài 4 trang 18 SGK Hóa 12
Làm bay hơi 7,4 gam một este A no, đơn chức thu được một thể tích hơi bằng thể tích của 3,2 gam khí oxi ở cùng điều kiện nhiệt độ, áp suất.
a) Tìm công thức phân tử của A.
b) Thực hiện phản ứng xà phòng hóa 7,4 gam A với dung dịch NaOH khi đến phản ứng hoàn toàn thu được sản phẩm có 6,8 gam muối. Tìm công thức cấu tạo và tên gọi của A.
Phương pháp giải
Để giải quyết các yêu cầu của đề bài, ta thực hiện các bước sau:
a) Công thức tổng quát của este no, đơn chức là CnH2nO2 (n≥2)
- Từ nO2 = nA → MA → n → Công thức phân tử.
b) Este đơn chức nên ta có: n muối = n este → M muối → Công thức cấu tạo của muối
→ Công thức cấu tạo của este.
Hướng dẫn giải
Câu a: Công thức phân tử của A
Vì A là este no, đơn chức nên có công thức phân tử là CnH2nO2
Ta có:
\(n_{A} = n_{O_{2}}= \frac{3,2}{32} =0,1 \ (mol)\)
⇒ MA = 74 g/mol ⇒ 14n + 32 = 74 ⇒ n = 3.
⇒ Công thức phân tử của A là C3H6O2
Câu b: Công thức cấu tạo của este
Gọi công thức phân tử của A là RCOOR'
Ta có phương trình hóa học:
RCOOR' + NaOH → RCOONa + R'OH
Theo phương trình
nRCOONa = nA = 7,4 : 74 = 0,1 (mol)
⇒ MRCOONa = 6,8 : 0,1 = 68 g/mol
⇒ R + 67 = 68 ⇒ R = 1
Vậy R là H (hay muối là HCOONa)
→ Công thức cấu tạo của A là HCOOC2H5 (etyl fomat).
5. Giải bài 5 trang 18 SGK Hóa 12
Khi thủy phân a gam một este X thu được 0,92 gam glixerol, 3,02 gam natri linoleat C17H31COONa và m gam natri oleat C17H33COONa.
Tính giá trị của a, m. Viết công thức cấu tạo có thể có của X.
Phương pháp giải
Đây là dạng bài thủy phân este trong môi trường kiềm, để giải quyết các yêu cầu của đề bài ta thực hiện các bước sau:
- Bước 1: Tính số mol của glixerol và natri lioleat công thức cấu tạo của X
- nC17H33COONa → m
- Bước 2: Từ số mol nX = nglixerol → a
Hướng dẫn giải
Phương trình hóa học tổng quát: (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Số mol glixerol = 0,92 : 92 = 0,01 mol
Theo tỉ lệ phản ứng ⇒ nmuối = nNaOH = 3.nglixerol = 3. 0,01 = 0,03 mol
Số mol n(C17H31COONa) = 3,02 : 302 = 0,01 mol
Vậy nC17H33COONa = 0,03 – 0,01 = 0,02 mol
⇒ m = mC17H33COONa = 0,02. 304 = 6,08(g)
mNaOH = 0,03. 40 = 1,2 g
Áp dụng định luật bảo toàn khối lượng ta có:
a = meste = mmuối + mglixerol - NaOH = 6,08 + 3,02 + 0,92 - 1,2 = 8,82 gam
Tỉ lệ nC17H31COONa : nC17H33COONa = 0,01 : 0,02 = 1:2
Vậy CTCT của X là C17H31COOC3H5(C17H33COO)2
6. Giải bài 6 trang 18 SGK Hóa 12
Thủy phân hoàn toàn 8,8 gam este đơn chức, mạch hở X với 100ml dung dịch KOH 1M (vừa đủ) thu được 4,6 gam một ancol Y. Tên gọi của X là
A. etyl fomat. B. etyl propionate.
C. etyl axetat. D. propyl axetat.
Phương pháp giải
Để xác định tên gọi của este, ta thực hiện các bước sau:
- Bước 1: Khi thủy phân este đơn chức với KOH vừa đủ ta luôn có: n este = nKOH = n ancol ⇒ M este
- Bước 2: Tính Mancol ⇒ Công thức cấu tạo của este ⇒ Tên gọi của X.
Hướng dẫn giải
Gọi CTPT của este là RCOOR1
Số mol KOH nKOH = 0,1.1 = 0,1 (mol)
RCOOR1 + KOH → RCOOK + R1OH
Theo pt: nRCOOR1 = nKOH = 0,1 mol.
Ta có:
CTCT của este là: CH3COOC2H5 (etyl axetat)
Đáp án C
7. Giải bài 7 trang 18 SGK Hóa 12
Đốt cháy hoàn toàn 3,7 gam một este đơn chức X thu được 3,36 lít khí CO2 (đktc) và 2,7 gam nước. Công thức phân tử của X là
A. C2H4O2. B. C3H6O2.
C. C4H8O2. D. C5H8O2.
Phương pháp giải
Để xác định công thức phân tử của X:
- Bước 1: nCO2 ⇒ nC, nH2O ⇒ nH, mO = mX-mC-mH ⇒ nO
- Bước 2: Suy ra tỉ lệ C:H:O ⇒ Công thức đơn giản nhất ⇒ Công thức phân tử.
Hướng dẫn giải
nCO2 = 3,36/22,4 = 0,15 mol ⇒ nC = 0,15 mol
nH2O = 2,7/18 = 0,15 mol ⇒ nH = 0,3 mol
mO = mX-mC-mH = 3,7 - 0,15.12 - 0,3.1 = 1,6 gam ⇒ nO= 0,1 mol
⇒ Tỉ lệ C:H:O = 0,15:0,3:0,1=3:6:2
⇒ CTĐGN C3H6O2
Mà este là đơn chức (chứa 2 nguyên tử O) ⇒ CTPT của X là C3H6O2
Đáp án B.
8. Giải bài 8 trang 18 SGK Hóa 12
10,4 gam hỗn hợp X gồm axit axetic và etyl axetat tác dụng vừa đủ với 150 gam dung dịch natri hiđroxit 4% . Phần trăm khối lượng của etyl axetat trong hỗn hợp bằng
A. 22% B. 42,3%
C. 57,7% D. 88%
Phương pháp giải
Để xác định phần trăm khối lượng của etyl axetat trong hỗn hợp:
- Bước 1: Đặt số mol mỗi chất trong X là x, y, viết phương trình hóa học
- Bước 2: Lập hệ 2 phương trình 2 ẩn dựa vào dữ kiện đề bài: mX, nNaOH
- Bước 3: Giải hệ phương trình ⇒ Phần trăm khối lượng.
Hướng dẫn giải
Gọi số mol của CH3COOH và CH3COOC2H5 lần lượt là x, y
CH3COOH + NaOH → CH3COONa
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH.
\(\\ n_{NaOH} = \frac{150.4}{100.40} = 0,15 \ (mol)\)
Ta có hệ phương trình:
\(\left\{ {\begin{array}{*{20}{c}}
{x + y = 0,15\;\;\;\;\;\;}\\
{60x + 88y = 10,4}
\end{array}} \right.\)
Giải hệ phương trình ta có x = 0,1; y = 0,05.
Khối lượng etyl axetat :
mCH3COOC2H5 = 88.0,05 = 4,4(g)
\(\% {m_{etyl\;axetat}} = \frac{{0,05.88}}{{10,4}} = 42,3\;\% \)
Đáp án B.



.PNG)
.PNG)
.PNG)
.PNG)
.PNG)
.PNG)